16.现有下列4组物质:
A.NaOH、Ca(OH)2、SO2、Fe(OH)3
B.Cl2、C、S、Cu
C.Hg、Cu、Zn、H2
D.H2O、HCl、H2SO4、HNO3
(1)填写下列空白:
(2)4组物质中都属于电解质的是D(填序号).
(3)写出实验室制备Cl2的离子方程式为MnO2+4H++2Cl-(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;.
A.NaOH、Ca(OH)2、SO2、Fe(OH)3
B.Cl2、C、S、Cu
C.Hg、Cu、Zn、H2
D.H2O、HCl、H2SO4、HNO3
(1)填写下列空白:
| A组 | B组 | C组 | D组 | |
| 分类标准 | 碱 | 常温下为固体 | 金属单质 | 酸 |
| 不属于该类别的物质 | SO2 | Cl2 | H2 | H2O |
(3)写出实验室制备Cl2的离子方程式为MnO2+4H++2Cl-(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;.
15.氯苯是燃料、医药、有机合成的中间体,是重要的有机化工产品.实验室制取氯苯如图1所示(加热和固定仪器的装置略去).
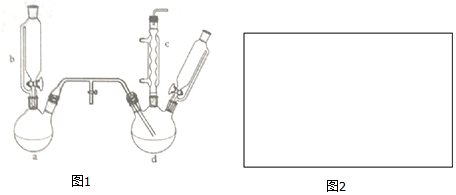
回答下列问题:
(1)a和b仪器组合成制取氯气的装置,反应无需加热,则a装置中的固体反应物可以是BC.(填序号)
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)把氯气通入反应器d中(d装置有FeCl3和苯),加热维持反应温度40-60℃,温度过高会生成过多的二氯苯.对d加热的方法是水浴加热.
(3)装置c的名称是(球形)冷凝管,装置c出口的气体成分有HCl、Cl2、水蒸气和苯蒸汽.
(4)制取氯苯的化学方程式为: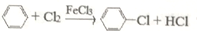 .
.
(5)装置d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.
①碱洗之前要水洗.其目的是洗去FeCl3、HCl等无机物.节省碱的用量,降低成本.
②10%NaOH溶液碱洗时发生氧化还原反应的化学反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.
(6)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸汽,请在图2中画出,并标明所用试剂.
(7)工业生产中苯的流失情况如表所示:
则10t 苯可制得成品氯苯$\frac{10×(1-0.0892)×112.5}{78}$t.(列出计算式即可.氯苯和苯的相对分子质量分别是112,5和78)

回答下列问题:
(1)a和b仪器组合成制取氯气的装置,反应无需加热,则a装置中的固体反应物可以是BC.(填序号)
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)把氯气通入反应器d中(d装置有FeCl3和苯),加热维持反应温度40-60℃,温度过高会生成过多的二氯苯.对d加热的方法是水浴加热.
(3)装置c的名称是(球形)冷凝管,装置c出口的气体成分有HCl、Cl2、水蒸气和苯蒸汽.
(4)制取氯苯的化学方程式为:
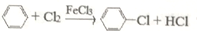 .
.(5)装置d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.
①碱洗之前要水洗.其目的是洗去FeCl3、HCl等无机物.节省碱的用量,降低成本.
②10%NaOH溶液碱洗时发生氧化还原反应的化学反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.
(6)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸汽,请在图2中画出,并标明所用试剂.
(7)工业生产中苯的流失情况如表所示:
| 项目 | 二氯苯 | 氯化尾气 | 蒸气 | 成品 | 不确定苯耗 | 合计 |
| 苯流失量(t/kg) | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
14.下列说法正确的是( )
| A. | “物质的量”是衡量物质重量的物理量 | |
| B. | 氢氧化钠的摩尔质量是40g | |
| C. | 物质的量浓度的常用单位是mol•L-1 | |
| D. | 1mol任何物质所占有的体积都是22.4L |
13.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 1mol H2O在标准状况下的体积为22.4 L | |
| D. | 1L 1mol•L-1K2SO4溶液中含有的钾离子数目为NA |
12.氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是( )
| A. | 铁在氯气中燃烧,生成棕红色的烟 | |
| B. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
11.下列有关物质用途的说法中,不正确的是( )
| A. | 硅可用于制造光导纤维 | |
| B. | 盛氢氧化钠溶液的试剂瓶不能用玻璃塞 | |
| C. | 氯气可用于制取漂白粉 | |
| D. | 氢氧化铝可用于制造中和胃酸的药剂 |
10.关于如图所示原电池装置的叙述,正确的是( )
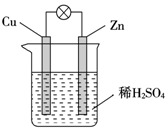

| A. | 电子从铜片经外电路流向锌 | B. | Zn为负极,Cu为正极 | ||
| C. | H+在铜片上得电子发生氧化反应 | D. | 该装置能将电能转化为化学能 |
9.下列物质与水反应生成强碱的是( )
| A. | Na2O | B. | SO3 | C. | CO2 | D. | NH3 |
8.有10g Na2O2、Na2O、Na2CO3、NaOH的混合物与100ml质量分数为2mol•L-1的盐酸恰好反应,蒸干溶液,最终得固体质量为( )
| A. | 11.7 g | B. | 5.85 g | C. | 8 g | D. | 15.5 g |
7.向含有下列离子的溶液中分别加入烧碱固体(体积变化忽略),离子浓度减小的是 ①Na+、②HCO3-、③Cl-、④Ca2+ ⑤NH4+ ⑥SO42-( )
0 161181 161189 161195 161199 161205 161207 161211 161217 161219 161225 161231 161235 161237 161241 161247 161249 161255 161259 161261 161265 161267 161271 161273 161275 161276 161277 161279 161280 161281 161283 161285 161289 161291 161295 161297 161301 161307 161309 161315 161319 161321 161325 161331 161337 161339 161345 161349 161351 161357 161361 161367 161375 203614
| A. | ②③④ | B. | ③④⑤ | C. | ②④⑥ | D. | ②④⑤ |