题目内容
11.下列有关物质用途的说法中,不正确的是( )| A. | 硅可用于制造光导纤维 | |
| B. | 盛氢氧化钠溶液的试剂瓶不能用玻璃塞 | |
| C. | 氯气可用于制取漂白粉 | |
| D. | 氢氧化铝可用于制造中和胃酸的药剂 |
分析 A.光导纤维的成分是二氧化硅;
B.氢氧化钠与二氧化硅反应生成硅酸钠,硅酸钠溶液具有粘性;
C.氯气与石灰乳反应生成漂白粉;
D.氢氧化铝具有弱碱性.
解答 解:A.光导纤维的成分是二氧化硅,不是硅单质,故A错误;
B.氢氧化钠与二氧化硅反应生成硅酸钠,硅酸钠溶液具有粘性,能把瓶塞和试剂瓶粘在一起,所以盛氢氧化钠溶液的试剂瓶不能用玻璃塞,故B正确;
C.氯气与石灰乳反应生成漂白粉,所以氯气可用于制取漂白粉,故C正确;
D.氢氧化铝具有弱碱性,能与胃酸中的HCl反应,对人体没有腐蚀性,所以氢氧化铝可用于制造中和胃酸的药剂,故D正确,
故选A.
点评 本题考查硅、铝及卤素化合物性质与用途,比较基础,旨在考查学生对基础知识的理解掌握,注意基础知识的识记积累.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
2.下列与有机物的结构、性质的有关叙述中正确的是( )
| A. | 天然油脂的主要成分是高级脂肪酸 | |
| B. | 分馏、干馏都是物理变化,裂化、裂解都是化学变化 | |
| C. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| D. | 乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| B. | 常温常压下,16gCH4所含中子数目为8NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA | |
| D. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
16.现有下列4组物质:
A.NaOH、Ca(OH)2、SO2、Fe(OH)3
B.Cl2、C、S、Cu
C.Hg、Cu、Zn、H2
D.H2O、HCl、H2SO4、HNO3
(1)填写下列空白:
(2)4组物质中都属于电解质的是D(填序号).
(3)写出实验室制备Cl2的离子方程式为MnO2+4H++2Cl-(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;.
A.NaOH、Ca(OH)2、SO2、Fe(OH)3
B.Cl2、C、S、Cu
C.Hg、Cu、Zn、H2
D.H2O、HCl、H2SO4、HNO3
(1)填写下列空白:
| A组 | B组 | C组 | D组 | |
| 分类标准 | 碱 | 常温下为固体 | 金属单质 | 酸 |
| 不属于该类别的物质 | SO2 | Cl2 | H2 | H2O |
(3)写出实验室制备Cl2的离子方程式为MnO2+4H++2Cl-(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;.
3.有一铁粉和氧化铜的混合物8.32g,进行如下实验:根据实验所得数据,有关说法正确的是( )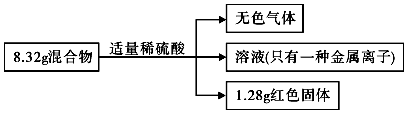

| A. | 无色气体的体积为2.24L | |
| B. | 原混合物中铁的质量为6.72g | |
| C. | 反应后的溶液中金属离子物质的量为0.02 mol | |
| D. | 反应消耗的H2SO4物质的量为0.1 mol |
20.物质的量浓度均为1mol/L的下列电解质溶液各取10mL混合后,pH小于7的是( )
| A. | Ba(OH)2、NaHSO4 | B. | Na2CO3、HNO3 | C. | NaHCO3、AlCl3 | D. | NaOH、CH3COOH |
5.下列选项中,互为同位素的是( )
| A. | 金刚石和石墨 | B. | CO和CO2 | C. | 16O和18O | D. | 1H216O和2H218O |
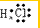 ;由两种元素组成的共价化合物的水溶液显碱性,这种化合物的结构式是
;由两种元素组成的共价化合物的水溶液显碱性,这种化合物的结构式是 .
. →
→ .
.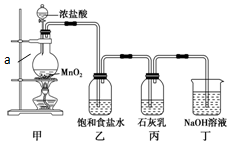 某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.
某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.