2.一种熔融碳酸盐燃料电池原理示意图如图.下列有关该电池的说法不正确的是( )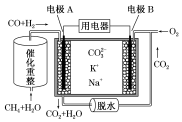

| A. | 反应CH4+H2O $\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1mol CH4转移6NA电子 | |
| B. | 电极A上H2参与的电极反应为H2+CO32--2e-=CO2+H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为O2+2CO2+4e-=2CO32- |
1.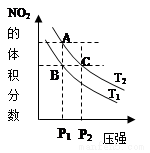 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 若恒温恒容时充入氩气,平衡向逆反应方向移动 | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | 由状态B到状态A,可以用加热的方法 | |
| D. | 因为B、C两点NO2的体积分数相同,所以化学平衡常数KB=KC. |
19.下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是( )
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸钙与盐酸 | CO32-+2H+=H2O+CO2↑ | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | 向次氯酸钙溶液通入过量CO2 | Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 正确 |
| C | 石灰水中滴加少量NaHCO3溶液 | Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误,不满足Ca(OH)2的配比 |
| D | 过量铁屑溶于稀硝酸 | 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |
18.NaNO2是一种食品添加剂,它与酸性KMnO4溶液可发生反应MnO4-+NO2-+H+→Mn2++NO3-+H2O(未配平).下列叙述中正确的是( )
| A. | 生成1 mol NaNO3需消耗0.4 mol KMnO4 | |
| B. | 反应过程中溶液的酸性增强 | |
| C. | 该反应中NO2-被还原 | |
| D. | H+可以是盐酸 |
17. 在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
 在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )| A. | Mg2+、Al3+、Fe2+ | B. | Mg2+、Al3+ | C. | H+、Ba2+、Al3+ | D. | H+、Mg2+、Al3+ |
16.下列物质中,与盐酸、氢氧化钠溶液均能反应,且都生成氢气的是( )
| A. | Al2O3 | B. | Fe | C. | Al | D. | (NH4)2CO3 |
15.常温下,能溶于浓HNO3的单质是( )
| A. | Al | B. | Fe | C. | Cu | D. | Si |
14.下列离子方程式的书写正确的是( )
| A. | Al2O3和NaOH溶液反应:Al2O3+2OH-=2AlO2-+H2↑ | |
| B. | 过氧化钠固体与水反应:2O22-+2H2O═4OH-+O2↑ | |
| C. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
13.在pH=1无色溶液中,能大量共存的离子组是( )
0 160945 160953 160959 160963 160969 160971 160975 160981 160983 160989 160995 160999 161001 161005 161011 161013 161019 161023 161025 161029 161031 161035 161037 161039 161040 161041 161043 161044 161045 161047 161049 161053 161055 161059 161061 161065 161071 161073 161079 161083 161085 161089 161095 161101 161103 161109 161113 161115 161121 161125 161131 161139 203614
| A. | Na+、OH-、Cl-、HCO3- | B. | K+、Cl-、Mg2+、SO42- | ||
| C. | Fe3+、Na+、NO3-、Al3+ | D. | Cl-、NH4+、Ag+、NO3- |