题目内容
16.下列物质中,与盐酸、氢氧化钠溶液均能反应,且都生成氢气的是( )| A. | Al2O3 | B. | Fe | C. | Al | D. | (NH4)2CO3 |
分析 结合物质的性质进行分析解答,既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的铵盐(如(NH4)2CO3等)、弱酸的酸式盐(NaHCO3、NaHS等)、单质(如Al)、氨基酸等.在金属活动顺序表中排在H前边的计算能与酸反应生成氢气,与强碱溶液反应生成氢气的物质有Al、Si等.
解答 解:A.氧化铝与盐酸反应生成氯化铝与水,与氢氧化钠溶液反应生成偏铝酸钠与水,没有氢气生成,故A不符合;
B.铁与盐酸反应生成氯化亚铁与氢气,铁与氢氧化钠溶液不反应,故B不符合;
C.铝与盐酸反应生成氯化铝与氢气,与氢氧化钠溶液反应生成偏铝酸钠与氢气,故C符合;
D.碳酸铵与盐酸反应生成氯化铵与二氧化碳、与氢氧化钠反应生成碳酸钠与氨气,没有氢气生成,故D不符合;
故选C.
点评 本题考查元素化合物的性质等,难度中等,注意概念总结能与酸、碱反应的物质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列说法正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 用加热的方法可除去KNO3溶液中混有的Fe3+ | |
| D. | Na2CO3溶液加水稀释后,恢复至室温,pH和KW均减小 |
7.胶体最本质的特征是( )
| A. | 丁达尔效应 | B. | 分散质颗粒直径在1nm~100nm之间 | ||
| C. | 布朗运动 | D. | 聚沉 |
4.下列化合物不能由单质直接化合生成的是( )
| A. | SO3 | B. | FeS | C. | Cu2S | D. | CuCl2 |
11.下列说法中,正确的是( )
| A. | SO2的摩尔质量是64 g | |
| B. | 标准状况下18 g水的体积是22.4 L | |
| C. | 14g N2含有的分子数为0.5NA | |
| D. | 1mol/LMgCl2溶液中含有Cl-的数目为2NA |
1.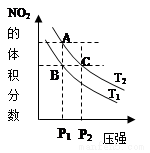 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 若恒温恒容时充入氩气,平衡向逆反应方向移动 | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | 由状态B到状态A,可以用加热的方法 | |
| D. | 因为B、C两点NO2的体积分数相同,所以化学平衡常数KB=KC. |
16.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 298K 101kP时,22.4L CO2所含的原子数为3NA | |
| B. | 1mol Cl2与足量的Fe完全反应,转移的电子数为2NA | |
| C. | 0.5mol C2H2和C6H6的气态混合物中所含原子总数为2NA | |
| D. | 2L 1mol/L的盐酸中所含HCl分子数约为2NA |