12.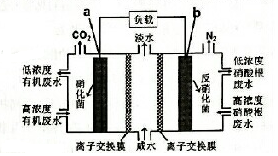 一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法的是( )
 一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法的是( )| A. | a电极为该电池的正极 | |
| B. | 电极b的反应式:2NO3--10e-+12H+=N2↑+6H2O | |
| C. | 每处理1molC8H10O5,b电极将产生3.2molN2 | |
| D. | a电极离子交换膜允许Na+白中间空迁有机废水处理室 |
11.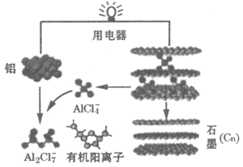 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 放电时,有机阳离子向铝电极方向移动 | |
| C. | 放电时的负极反应为:Al-3e-+7AlCl4-═4Al2Cl7- | |
| D. | 充电时,AlCl4-向石墨电极方向移动 |
10.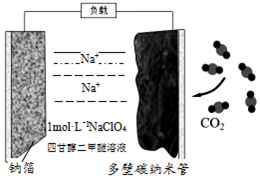 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )| A. | 充电时,钠箔与外接电源的负极相连 | |
| B. | 电池工作温度可能在200℃以上 | |
| C. | 放电时,Na+向正极移动 | |
| D. | 放电时,正极的电极反应为:4Na++3CO2+4e-=2Na2CO3+C |
9.K2FeO4可与水发生反应4K2FeO4+10H2O=4Fe(OH)3(胶体)+8KOH+3O2↑.下列说法正确的是( )
| A. | 氧化性:K2FeO4<O2 | |
| B. | K2FeO4可用作自来水的消毒剂和净水剂 | |
| C. | K2FeO4可用作碱性K2FeO4-Zn电池的负极材料 | |
| D. | 常温常压下,该反应每生成22.4L O2,转移电子的数目为4×6.02×1023个 |
8.氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池.氢镍电池的总反应式是:$\frac{1}{2}{H_2}+NiOOH$$?_{放电}^{充电}$Ni(OH)2据此反应式判断,下列叙述中不正确的是( )
| A. | 电池放电时,电池负极周围溶液的PH不断增大 | |
| B. | 电池放电时,正极的电极反应为:NiOOH+e-+H2O=Ni(OH)2+OH- | |
| C. | 电池充电时,阳极周围溶液的PH不断减小 | |
| D. | 电池充电时,阴极的电极反应为:2H2O+2e-=H2+2OH- |
7.现有部分被氧化的Cu-Fe合金粉末8.96g,将其进行如下处理

下列说法正确的是( )

下列说法正确的是( )
| A. | 滤渣B中一定含有Cu,可能含有Fe | |
| B. | 向滤液C中滴入KSCN溶液,溶液可能变红色 | |
| C. | 合金粉末中可能含5.68gCuO | |
| D. | 气体A在标准状况下的体积为224mL |
6.下列物质中的硫元素,只具有还原性而不具有氧化性的是( )
| A. | H2S | B. | SO2 | C. | H2SO3 | D. | H2SO4 |
5.可溶性铝盐与强碱溶液反应,铝元素的存在形式如图,则a、b的差值为( )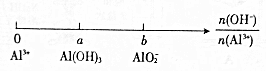
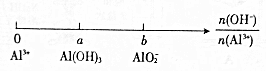
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
3.一定条件下反应 2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
0 160903 160911 160917 160921 160927 160929 160933 160939 160941 160947 160953 160957 160959 160963 160969 160971 160977 160981 160983 160987 160989 160993 160995 160997 160998 160999 161001 161002 161003 161005 161007 161011 161013 161017 161019 161023 161029 161031 161037 161041 161043 161047 161053 161059 161061 161067 161071 161073 161079 161083 161089 161097 203614
| A. | 容器中各组分的物质的量不随时间变化 | |
| B. | 容器内三种气体 AB、A2、B2共存 | |
| C. | 2v正(AB)=v逆(A2) | |
| D. | 单位时间内消耗n mol A2,同时生成2n mol AB |