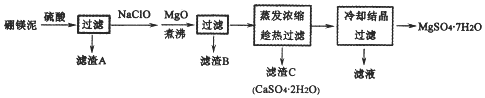
6.下列各组离子在溶液中能够大量共存的是( )
| A. | NH4+、Ca2+、OH-、HCO3- | B. | NH4+、Br-、Na+、SO42- | ||
| C. | Ag+、H+、SO32-、ClO- | D. | H+、Cl-、Fe2+、CO32- |
5.分类法是一种行之有效、简单易行的科学方法.某同学用下表所示对所学知识进行分类,其中甲与乙、丙、丁是包含关系.下列各组中,正确的组合是( )
| 选项 | 甲 | 乙、丙、丁 |
| A | 纯净物 | 液氯、KAl(SO4)2、CuSO4•5H2O |
| B | 能导电 | Fe、NaCl晶体、AgCl |
| C | 碱 | 一水合氨、NaOH、纯碱 |
| D | 电解质 | 盐酸、硫酸、硝酸 |
| A. | A | B. | B | C. | C | D. | D |
4. 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图: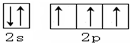 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)N>O>C.
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)H2O,原因是水分子间可以形成氢键,使沸点升高.
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:C≡O.
(5)R的一种配合物的化学式为RCl3•6H2O.已知0.01mol RCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3B.[R(H2O)5Cl]Cl2•H2O
C.[R(H2O)4Cl2]Cl•2H2OD.[R(H2O)3Cl3]•3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,继续滴加氨水至过量,沉淀溶解,
得到天蓝色溶液,写反应的离子方程式为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
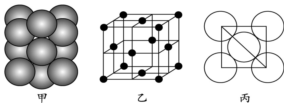
(7)元素E的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).
 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 原子核外的L层有3个未成对电子 |
| Z | 地壳中含量最多的元素 |
| Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | N能层上只有一个电子,K、L、M层均排满电子 |
(1)写出元素Y的原子核外价电子排布图:
 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)N>O>C.
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)H2O,原因是水分子间可以形成氢键,使沸点升高.
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:C≡O.
(5)R的一种配合物的化学式为RCl3•6H2O.已知0.01mol RCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3B.[R(H2O)5Cl]Cl2•H2O
C.[R(H2O)4Cl2]Cl•2H2OD.[R(H2O)3Cl3]•3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,继续滴加氨水至过量,沉淀溶解,
得到天蓝色溶液,写反应的离子方程式为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
(7)元素E的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).
3.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
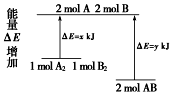

| A. | 该反应的反应热△H=x-y kJ/mol | |
| B. | 断裂1 mol A-A键和1 mol B-B键放出x kJ能量 | |
| C. | 2 mol AB的总能量高于1 mol A2和1 mol B2总能量 | |
| D. | 该反应是吸热反应 |
2.绿色能源是指使用过程中不排放或排放极少污染物的能源.下列属于绿色能源的是( )
①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材 ⑦地热能.
①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材 ⑦地热能.
| A. | ①②③⑤ | B. | ②④⑤⑥ | C. | ③④⑤⑦ | D. | ①②⑤⑦ |
1.某原子的一种激发态为1s22s12p1,则该元素在周期表中的位置为( )
| A. | 第二周期ⅡA族 | B. | 第二周期ⅢA族 | C. | 第二周期ⅠA族 | D. | 第二周期ⅣA族 |
20.在多电子原子中,决定轨道能量的是( )
| A. | 电子层 | B. | 电子层和能级 | ||
| C. | 电子层、能级和原子轨道空间分布 | D. | 原子轨道空间分布和电子自旋方向 |
18.如图为一种微生物燃料电池结构示意图,下列叙述正确的是( )
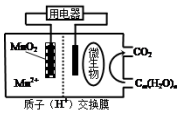

| A. | 放电过程中,电子从正极转移到负极 | |
| B. | 放电过程中,H+从正极区移向负极区 | |
| C. | 正极反应式为:MnO2+4H++2e-=Mn2++2H2O | |
| D. | 若Cm(H2O)n是葡萄糖,当电路中转移了6NA电子时,消耗的葡萄糖是1mol |
17.下列实验能达到预期目的是( )
0 160778 160786 160792 160796 160802 160804 160808 160814 160816 160822 160828 160832 160834 160838 160844 160846 160852 160856 160858 160862 160864 160868 160870 160872 160873 160874 160876 160877 160878 160880 160882 160886 160888 160892 160894 160898 160904 160906 160912 160916 160918 160922 160928 160934 160936 160942 160946 160948 160954 160958 160964 160972 203614
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 室温下,用pH试纸分别测定浓度为18mol/L和0.1mol/L H2SO4溶液的pH | 比较不同浓度H2SO4的酸性强弱 |
| C | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
| D | 向10mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp>Ksp |
| A. | A | B. | B | C. | C | D. | D |