题目内容
18.如图为一种微生物燃料电池结构示意图,下列叙述正确的是( )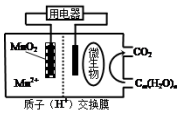
| A. | 放电过程中,电子从正极转移到负极 | |
| B. | 放电过程中,H+从正极区移向负极区 | |
| C. | 正极反应式为:MnO2+4H++2e-=Mn2++2H2O | |
| D. | 若Cm(H2O)n是葡萄糖,当电路中转移了6NA电子时,消耗的葡萄糖是1mol |
分析 形成原电池时,微生物所在电极区发生氧化反应,Cm(H2O)n被氧化生成水和二氧化碳,MnO2被还原生成Mn2+,为原电池的正极,放电时,阳离子向正极移动,阴离子向负极移动,电子从负极转移到正极,以此解答.
解答 解:A.放电过程中,电子从负极转移到正极,故A错误;
B.原电池工作时,阳离子向正极移动,阴离子向负极移动,所以H+从负极区移向正极区,故B错误;
C.MnO2被还原生成Mn2+,为原电池的正极,电极方程式为MnO2+4H++2e-═Mn2++2H2O,故C正确;
D.若Cm(H2O)n是葡萄糖,C元素化合价可认定为0价,当电路中转移了6NA电子时,反应的葡萄糖的物质的量为0.25mol,故D错误.
故选C.
点评 本题考查新型电池,为高频考点,题目难度不大,注意把握原电池的工作原理以及电极反应式的书写,解答本题的关键是根据物质的性质判断原电池的正负极.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
8.下列叙述正确的是( )
| A. | 用冰冷却苯,苯可以凝结成无色的晶体 | |
| B. | 苯与溴水混合后因发生反应而使溴水褪色 | |
| C. | 在苯中加入酸性 KMnO4 溶液,振荡后静置,上层液体为紫红色 | |
| D. | 1 mol 苯能与 3 mol H2发生加成反应,说明在苯环中含有 3 个双键 |
9. 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )| A. | “吸入”CO2时,钠箔为正极 | |
| B. | “呼出”CO2时,Na+向多壁碳纳米管电极移动 | |
| C. | “吸入”CO2时的正极反应:4Na++3CO2+4e-═2Na2CO3+C | |
| D. | 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol |
6.下列实验操作以及实验现象完全一致的是( )
| A | 向硫酸铜溶液中加入一小块金属钠 | 有红色固体析出 |
| B | 向饱和碳酸钠溶液中通入过量CO2气体 | 有白色细小晶体析出 |
| C | 将新制氯水滴到蓝色石蕊试纸上 | 试纸变红 |
| D | 将用砂子打磨过的铝箔置于酒精灯火焰上加热 | 铝熔化并滴落 |
| A. | A | B. | B | C. | C | D. | D |
13.乙烷混有乙烯,欲除去乙烯得到纯净干燥的乙烷,下列方法正确的( )
| A. | 依次通过溴水、烧碱、浓硫酸 | B. | 依次通过酸性KMnO4溶液、浓硫酸 | ||
| C. | 依次通过澄清石灰水、浓硫酸 | D. | 通入氢气,在一定条件下反应 |
3.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
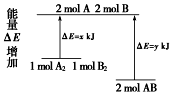

| A. | 该反应的反应热△H=x-y kJ/mol | |
| B. | 断裂1 mol A-A键和1 mol B-B键放出x kJ能量 | |
| C. | 2 mol AB的总能量高于1 mol A2和1 mol B2总能量 | |
| D. | 该反应是吸热反应 |
10.把一定量的铁铝合金平均分为两份,分别与足量硫酸和氢氧化钠溶液反应,结果放出H2的物质的量之比是3:1,则合金中铁与铝的物质的量之比为( )
| A. | 3:1 | B. | 1:3 | C. | 3:2 | D. | 2:3 |
8.中药狼巴草的成分之一M具有清炎杀菌作用,M的结构简式如图所示: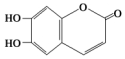 ,下列叙述正确的是( )
,下列叙述正确的是( )
 ,下列叙述正确的是( )
,下列叙述正确的是( )| A. | M的分子式为C9H6O4 | |
| B. | 1 mol M最多能与2 mol Br2发生反应 | |
| C. | 1 molM最多能与4 mol氢氧化钠反应 | |
| D. | M既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
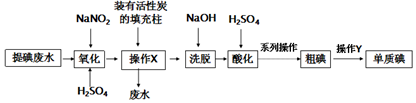
 请回答:
请回答: