11.下列离子方程式正确的是( )
| A. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-═H2O+CO2↑ | |
| D. | 将氯气通入KBr溶液中:Cl2+2Br-═2Cl-+Br2 |
10.下列说法中正确的是( )
| A. | 自然界中不存在游离态的硫 | |
| B. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 | |
| C. | 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 | |
| D. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 |
9.根据:2Fe3++2I-=2Fe2++I2;Br2+2Fe2+=2Fe3++2Br-两个反应,判断Fe3+、I2、Br2的氧化性顺序为( )
| A. | I2>Fe3+>Br2 | B. | Br2>I2>Fe3+ | C. | Br2>Fe3+>I2 | D. | Fe3+>Br2>I2 |
8.镁在CO2含量较多的空气里燃烧的产物是( )
| A. | MgO | B. | MgO和C | C. | MgO、Mg3N2 | D. | MgO、Mg3N2 和C |
7.下列说法正确的是( )
| A. | 用试管夹夹试管应从试管底往上套,拇指按在试管夹的短柄上 | |
| B. | 装碘的试剂瓶中残留的碘可以用酒精洗涤 | |
| C. | 配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用滴管滴加蒸馏水到刻度线 | |
| D. | 定容时,俯视刻度线,会使所配溶液的浓度偏低 |
5. 室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示:
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示:
(1)HB溶液体积稀释到1000毫升时,溶液中c(H+)=10-3mol/L.
(2)由图可判断:HA的酸性>(填“>”或“<”)HB的酸性.
(3)pH均为2的一元酸HA和HB各1mL,分别加水稀释后pH不同的原因是什么?请进行完整说明
.
 室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示:
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如图所示:(1)HB溶液体积稀释到1000毫升时,溶液中c(H+)=10-3mol/L.
(2)由图可判断:HA的酸性>(填“>”或“<”)HB的酸性.
(3)pH均为2的一元酸HA和HB各1mL,分别加水稀释后pH不同的原因是什么?请进行完整说明
| 物质 | 稀释中变化 | 稀释中n(H+)变化 | 稀释中c(H+)减小程度 |
| HA | HA=H++A-不移动 | 不变 | 大 |
| HB | HB?H++B- 正向移动 | 增加 | 小 |
4.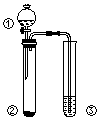 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 |
| C | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
3.已知可用Co2O3代替MnO2制备Cl2,反应后Co元素以 Co2+的形式存在.下列叙述不正确的是( )
| A. | 该反应中氧化性:Co2O3>Cl2 | |
| B. | 参加反应的HCl全部被Co2O3氧化 | |
| C. | 每生成1摩尔氯气,消耗1摩尔Co2O3 | |
| D. | 制备相同量的氯气,所需Co2O3质量比MnO2多 |
2.N2(g)与H2(g)在铁催化剂表面经历如图过程生成NH3(g):下列说法不正确的是( )

0 160743 160751 160757 160761 160767 160769 160773 160779 160781 160787 160793 160797 160799 160803 160809 160811 160817 160821 160823 160827 160829 160833 160835 160837 160838 160839 160841 160842 160843 160845 160847 160851 160853 160857 160859 160863 160869 160871 160877 160881 160883 160887 160893 160899 160901 160907 160911 160913 160919 160923 160929 160937 203614

| A. | Ⅰ过程中破坏的均为非极性键 | |
| B. | Ⅰ过程吸收能量,II过程放出能量 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H=-44 kJ•mol-1 | |
| D. | 1mol N2(g)与3 mol H2(g)所具有的总能量比2 mol NH3(g) 所具有的总能量高 |
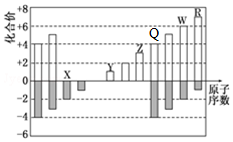 部分短周期元素化合价与原子序数的关系可用图表示.
部分短周期元素化合价与原子序数的关系可用图表示.