题目内容
9.根据:2Fe3++2I-=2Fe2++I2;Br2+2Fe2+=2Fe3++2Br-两个反应,判断Fe3+、I2、Br2的氧化性顺序为( )| A. | I2>Fe3+>Br2 | B. | Br2>I2>Fe3+ | C. | Br2>Fe3+>I2 | D. | Fe3+>Br2>I2 |
分析 根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性来解答.
解答 解:2Fe3++2I-=2Fe2++I2中,I元素的化合价升高,Fe的化合价降低,则氧化性:Fe3+>I2;
Br2+2Fe2+=2Fe3++2Br-中,Fe元素的化合价升高,Br的化合价降低,则氧化性:Br2>Fe3+,
所以离子的氧化性顺序为:Br2>Fe3+>I2;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及氧化还原反应中规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.H2S在O2中不完全燃烧生成S和H2O,下列说法中正确的是( )
| A. | 微粒半径:O2->S2- | B. | 还原性:H2S<H2O | ||
| C. | 稳定性:H2S<H2O | D. | 电离方程式:H2S?2H++S2- |
20.下列分子或离子中,中心原子不是sp3杂化的是( )
| A. | SO42- | B. | NO3- | C. | CH4 | D. | H2S |
17.下列物质间的转化不能通过一步反应实现的是( )
| A. | SiO2→H2SiO3 | B. | HClO→O2 | C. | Fe→FeCl2 | D. | Cu→CuSO4 |
4.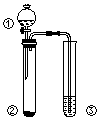 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 |
| C | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L的H2O中含有H-O键数目为NA | |
| B. | 常温下,1LpH=1的H2SO4溶液中电离产生的H+数为0.2NA | |
| C. | 6.4g SO2中空气中充分氧化,转移的电子数为0.2 NA | |
| D. | 0.1mol MnO2与足量的浓HCl加热反应产生的Cl2分子数为0.1NA |
3.不可能使溴水褪色的是( )
| A. | 己烯 | B. | 氢氧化钾溶液 | C. | 二氧化硫 | D. | 己烷 |