18.下列关于物质性质的表述正确的是( )
| A. | 向含有少量KSCN的FeI2溶液中滴加少量溴水,溶液出现血红色 | |
| B. | 用NH4HCO3固体以及其他固体药品能制得纯净的NH3 | |
| C. | 将SO2通入酸性KMnO4溶液中,溶液褪色,体现了SO2的漂白性 | |
| D. | 加热条件下,过量的Fe与浓硫酸反应只生成SO2一种气体 |
15.在2L密闭容器中加热0.1molN2O5,发生反应:N2O5(g)?N2O3(g)+O2(g),N2O3(g)?N2O(g)+O2(g).达到平衡时,n(N2O3)为0.02mol,n(02)为0.14mol,则c(N2O)为( )
| A. | 0.07mol•L-1 | B. | 0.06 mol•L-1 | C. | 0.04 mol•L-1 | D. | 0.03 mol•L-1 |
14.物质的量浓度相同的下列溶液中,NH4+浓度最大的是( )
| A. | NH4Cl | B. | NH4HSO4 | C. | CH3COONH4 | D. | (NH4)2Fe(SO4)2 |
13.下列说法不正确的是( )
| A. | 可以利用铝热反应冶炼高熔点的金属 | |
| B. | 现代石油化工,采作银作催化剂可以实现一步完成乙烯转化为环氧乙烷的过程,该反应的原子利用率为100% | |
| C. | 工业上制溴是向酸化的浓缩海水中直接通入氯气置换出溴即可 | |
| D. | 煤直接液化可得液体燃料 |
12.Li-SOCl2电池是迄今具有最高能量比的电池.该电池中锂为负极,碳棒为正极,无水四氯铝酸锂(LiAlCl4)的SOCl2溶液为电解液.电池总反应为电池的总反应可表示为:4Li+2SOCl2=4LiCl+SO2+S.下列说法不正确的是( )
| A. | 负极的电极反应式为 Li-e-=Li+ | |
| B. | 正极的电极反应式为2SOCl2+4e-=SO2+S+4Cl- | |
| C. | 若电解液中含有水,则该电池的效率将大大降低 | |
| D. | 若负极有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023 |
11.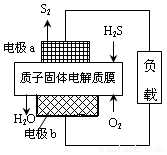 工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
 工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为O2+4H++4e-=2H2O | |
| C. | 若电路中通过2mol电子,则电池内部释放632kJ热能 | |
| D. | 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区 |
10.下列有关0.10mol•L-1的NH4Cl溶液的叙述不正确的是( )
| A. | c(H+)>c(OH-) | B. | c(NH4+)>c(Cl-) | ||
| C. | c(NH4+)+c(H+)=c(Cl-)+c(OH-) | D. | c(NH4+)+c(NH3.H2O)=0.10mol•L-1 |
9.某新型蓄电池放电、充电时的反应为Fe+Ni2O3+3H2O$?_{充电}^{放电}$Fe(OH)2+2Ni(OH)2.下列推断中不正确的是( )
0 160710 160718 160724 160728 160734 160736 160740 160746 160748 160754 160760 160764 160766 160770 160776 160778 160784 160788 160790 160794 160796 160800 160802 160804 160805 160806 160808 160809 160810 160812 160814 160818 160820 160824 160826 160830 160836 160838 160844 160848 160850 160854 160860 160866 160868 160874 160878 160880 160886 160890 160896 160904 203614
| A. | 充电时,Ni(OH)2为阳极 | |
| B. | 放电时,Fe为正极,Ni2O3为负极 | |
| C. | 该新型蓄电池的电解质溶液呈碱性 | |
| D. | 充电时,阴极反应式为Fe(OH)2+2e-=Fe+2OH- |
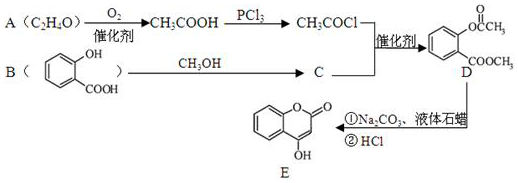
 .
.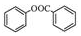 )的合成路线(无机原料任选).
)的合成路线(无机原料任选). .
. 如图为KNO3和NaCl的溶解度曲线,请回答下列问题:
如图为KNO3和NaCl的溶解度曲线,请回答下列问题: