题目内容
12.Li-SOCl2电池是迄今具有最高能量比的电池.该电池中锂为负极,碳棒为正极,无水四氯铝酸锂(LiAlCl4)的SOCl2溶液为电解液.电池总反应为电池的总反应可表示为:4Li+2SOCl2=4LiCl+SO2+S.下列说法不正确的是( )| A. | 负极的电极反应式为 Li-e-=Li+ | |
| B. | 正极的电极反应式为2SOCl2+4e-=SO2+S+4Cl- | |
| C. | 若电解液中含有水,则该电池的效率将大大降低 | |
| D. | 若负极有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023 |
分析 根据放电时分析反应的化合价变化,可得Li为还原剂,SOCl2为氧化剂,负极材料为Li(还原剂),发生氧化反应,电极反应式为Li-e-=Li+,正极发生还原反应,电极方程式为:2SOCl2+4e-=4Cl-+S+SO2,因为构成电池的两个主要成份Li能和氧气水反应,且SOCl2也与水反应,而充电过程刚好是逆过程,综合分析解答.
解答 解:A.放电时,负极上失电子发生氧化反应,电极反应式为Li-e-=Li+,故A正确;
B.正极发生还原反应,电极方程式为:2SOCl2+4e-=4Cl-+S+SO2,故B正确;
C.因为构成电池的两个主要成份Li能和水反应,且SOCl2也与水反应,若电解液中含有水,则不能形成原电池,故C错误;
D.负极电极反应式为Li-e-=Li+,有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023,故D正确;
故选C.
点评 本题考查化学电源新型电池,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
2.实验是化学研究的基础,如图装置或操作正确的是( )
| A. | 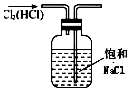 用图所示装置可得到纯净的Cl2 | |
| B. | 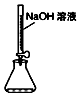 用图量取15.00mL的NaOH溶液 | |
| C. | 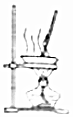 用图所示装置蒸发FeCl3溶液制备无水FeCl2 | |
| D. |  关闭分液漏斗的活塞,从b处加水,以检查装置的气密性 |
3.下列说法正确的是( )
| A. | 常温常压下,16g O3所含的氧原子数目为NA | |
| B. | 标准状况下,O2的体积取决于O2分子间的距离 | |
| C. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| D. | 若气体摩尔体积为22.4 L/mol,则所处条件为标准状况 |
20.某同学采用硫铁矿焙烧取硫后的烧渣 (主要成分为 Fe2O3、SiO2、Al2O3,不考虑其他 杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如图流程:下列说法不正确的是( )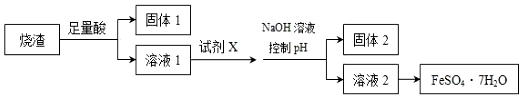

| A. | 溶解烧渣选用足量硫酸,试剂 X 选用铁粉 | |
| B. | 固体1 中一定含有 SiO2,控制 pH 是为了使 Al3+转化为 Al(OH)3,进入固体 2 | |
| C. | 从溶液 2 得到 FeSO4•7H2O 产品的过程中,须控制条件防止其氧化和分解 | |
| D. | 若改变方案,在溶液 1 中直接加 NaOH 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 FeSO4•7H2O |
7.在隔绝空气的条件下发生反应:CH4(g)=C(g)+2H2(g)△H>0,下列说法正确的是( )
| A. | 低温下是非自发反应,高温下是自发反应 | |
| B. | 任何温度下都是自发反应 | |
| C. | 低温下是自发反应,高温下是非自发反应 | |
| D. | 任何温度下都是非自发反应 |
4.醇类在我们的日常生话中扮演着重要的角色,下列对于醇类的认识正确的是( )
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 醇都可以发生消去反应 | |
| C. | 醇在Cu催化作用下都可以催化氧化 | |
| D. | 饱和一元脂肪醇的化学式可用通式CnH2n+2O表示 |
15.下列关于化学平衡常数的说法中,正确的是( )
| A. | 在任何条件下,化学平衡常数都是一个定值 | |
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 | |
| C. | 化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 | |
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
16.下列变化过程一定需要加入还原剂的是( )
| A. | KClO3→KCl | B. | KCl→AgCl | C. | H+→H2 | D. | C→CO2 |
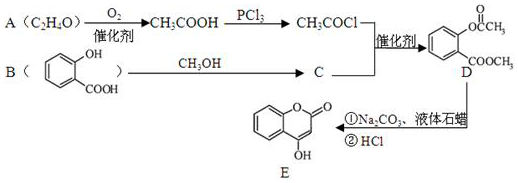
 .
.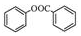 )的合成路线(无机原料任选).
)的合成路线(无机原料任选). .
.