15.某同学做如表实验:下列说法正确的是( )
| 装 置 | 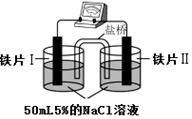 | 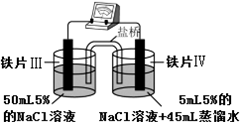 |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 铁片Ⅳ的电极反应式可能为Fe-3e-=Fe3+ | |
| C. | 用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极 | |
| D. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等 |
14. 已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
 已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| A. | 如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | a、b、c三点所示溶液中水的电离程度c>a>b | |
| D. | 图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a |
13.下列说法正确的是( )
| A. | BaSO4难溶于水,所以BaSO4是非电解质 | |
| B. | 弱电解质的导电性一定比强电解质弱 | |
| C. | 25℃时0.1mol/L的CH3COOH溶液pH=3,说明CH3COOH为弱电解质 | |
| D. | 某物质能导电,所以该物质一定是电解质 |
12.下列叙述正确的是( )
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,在等体积、等浓度的硝酸中加入氨水,溶液的导电性增强 | |
| C. | 25℃时,0.1mol/L的硫化氢溶液与等浓度的硫化钠溶液的导电能力相当 | |
| D. | 25℃时,将等体积PH=1的盐酸和水混合,混合后溶液的PH=1.3 |
11.下列说法正确的是( )
| A. | 正反应是放热反应的可逆反应,升高温度v(正)>v(逆) | |
| B. | 升高温度或使用催化剂是通过增加活化分子百分数而使反应速率加快 | |
| C. | 勒夏特列原理只使用于可逆反应,不使用于溶解和弱电解质的电离 | |
| D. | △G=△H-T△S适合任意条件的化学反应进行的方向判据 |
10.下列说法错误的是( )
| A. | 乙烷光照下能与浓盐酸发生取代反应 | |
| B. | 乙烯可以用作生产食品包装材料的原料 | |
| C. | 乙醇室温下在水中的溶解度大于溴乙烷 | |
| D. | 乙酸和甲酸甲酯互为同分异构体 |
9.醋酸的电离方程式是CH3COOH?H++CH3COO-,其电离常数表达式是Ka=$\frac{c(C{H}_{3}CO{O}^{-})×c({H}^{+})}{c(C{H}_{3}COOH)}$.
8.(1)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②反应一段时间后,实验A中的金属呈灰黑色,实验E中的金属呈紫红色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(2)在100℃和200kPa的条件下,反应aA(g)?bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维持温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度.
根据表中的数据,回答下列问题:
①压强从200kPa增加到500kPa时,平衡不移动(填“正向”“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
②压强从500kPa增加到1 000kPa时,平衡正向转移(填“正向”“逆向”或“不”),其原因可能是加压至1000kPa时,C物质变成了非气态物质.
 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②反应一段时间后,实验A中的金属呈灰黑色,实验E中的金属呈紫红色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(2)在100℃和200kPa的条件下,反应aA(g)?bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维持温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度.
| 压强(kPa) | 200 | 500 | 1 000 |
| B的浓度(mol•L-1) | 0.04 | 0.1 | 0.27 |
①压强从200kPa增加到500kPa时,平衡不移动(填“正向”“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
②压强从500kPa增加到1 000kPa时,平衡正向转移(填“正向”“逆向”或“不”),其原因可能是加压至1000kPa时,C物质变成了非气态物质.
7.下列说法不正确的是( )
| A. | 假说经过反复验证和修正,才发展成为科学的理论 | |
| B. | 研究物质的性质常用观察、实验、分类、比较等方法 | |
| C. | 在研究原子结构的过程中建立起的各种模型属于思维模型 | |
| D. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
6.0.1mol•L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是( )
①电离程度增大 ②c(NH3•H2O)增大 ③NH4+数目增多 ④c(OH-)增大 ⑤导电性增强.
0 159890 159898 159904 159908 159914 159916 159920 159926 159928 159934 159940 159944 159946 159950 159956 159958 159964 159968 159970 159974 159976 159980 159982 159984 159985 159986 159988 159989 159990 159992 159994 159998 160000 160004 160006 160010 160016 160018 160024 160028 160030 160034 160040 160046 160048 160054 160058 160060 160066 160070 160076 160084 203614
①电离程度增大 ②c(NH3•H2O)增大 ③NH4+数目增多 ④c(OH-)增大 ⑤导电性增强.
| A. | ①②③ | B. | ①③⑤ | C. | ①③ | D. | ②④ |