题目内容
15.某同学做如表实验:下列说法正确的是( )| 装 置 | 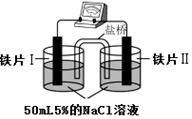 | 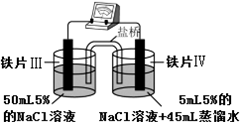 |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 铁片Ⅳ的电极反应式可能为Fe-3e-=Fe3+ | |
| C. | 用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极 | |
| D. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等 |
分析 对比两个盐桥的双液装置,图1中因两溶液中氯化钠的浓度相等,因此发生的是普通的化学腐蚀,且腐蚀速率相等,图2中因两溶液中氯化钠的浓度不相等,因此发
生的是电化学腐蚀,且浓度大的一极发生的反应是Fe-2e-=Fe2+,可以用K3[Fe(CN)6]溶液检验.
解答 解:A、图1中因两溶液中氯化钠的浓度相等,因此发生的是普通的化学腐蚀,且腐蚀速率相等,电流计指针未发生偏转,铁片Ⅰ、铁片Ⅱ均被腐蚀,故A错误;
B、铁片Ⅳ的电极反应式为Fe-2e-=Fe2+,故B错误;
C、图2中因两溶液中氯化钠的浓度不相等,因此发生的是电化学腐蚀,且浓度大的一极发生的反应是Fe-2e-=Fe2+,可以用K3[Fe(CN)6]溶液检验亚铁离子的存在,进而判断电池的正、负极,故C正确;
D、铁片Ⅰ、Ⅲ所处的电解质溶液浓度不相同,二者的腐蚀速率不相等,故D错误;
故选C.
点评 本题考查了原电池原理的分析应用,电极反应和电极判断,注意原电池的构成条件和原理是解题关键,题目难度中等.

练习册系列答案
相关题目
5. 已知反应:3I-(aq)+S2O82-(aq)═I3-(aq)+2SO42-(aq)+Q
已知反应:3I-(aq)+S2O82-(aq)═I3-(aq)+2SO42-(aq)+Q
(1)写出反应的平衡常数表达式:K=$\frac{{c}^{2}(S{{O}_{4}}^{2-})c({{I}_{3}}^{-})}{{c}^{3}({I}^{-})c({S}_{2}{{O}_{8}}^{2-})}$.
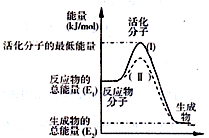
(2)如图表示反应过程中有关物质的能量,则反应过程中的Q>0(填>、<、=);(I)、(II)两曲线中,使用催化剂的是(II)曲线.
(3)反应的速率可以用I3-与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大.如表是在20℃进行实验时所记录的数据
从表中数据分析,该实验的目的是研究I-、S2O82-浓度对反应速率的影响;表中显色时间t1=22s;最终得出的结论是反应速率与反应物浓度乘积成正比.
 已知反应:3I-(aq)+S2O82-(aq)═I3-(aq)+2SO42-(aq)+Q
已知反应:3I-(aq)+S2O82-(aq)═I3-(aq)+2SO42-(aq)+Q(1)写出反应的平衡常数表达式:K=$\frac{{c}^{2}(S{{O}_{4}}^{2-})c({{I}_{3}}^{-})}{{c}^{3}({I}^{-})c({S}_{2}{{O}_{8}}^{2-})}$.
(2)如图表示反应过程中有关物质的能量,则反应过程中的Q>0(填>、<、=);(I)、(II)两曲线中,使用催化剂的是(II)曲线.
(3)反应的速率可以用I3-与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大.如表是在20℃进行实验时所记录的数据
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
6.下列说法中正确的是( )
| A. | 分子组成相差一个或几个CH2原子团的有机物是同系物 | |
| B. | 各组成元素质量分数相同的烃是同一种烃 | |
| C. | 分子式相同而结构式不同的有机物一定是同分异构体 | |
| D. | 具有相同通式且相差一个或若干个CH2原子团的有机物一定是同系物 |
3.下列实验操作正确的是( )
| A. | 将含硫酸的废液倒入水槽,用水冲入下水道 | |
| B. | 对医用酒精进行蒸馏操作可得到更高纯度的酒精溶液 | |
| C. | 加热高锰酸钾固体制取并收集氧气结束后,应立即停止加热 | |
| D. | 蒸馏实验时,冷水应从上口进下口出 |
10.下列说法错误的是( )
| A. | 乙烷光照下能与浓盐酸发生取代反应 | |
| B. | 乙烯可以用作生产食品包装材料的原料 | |
| C. | 乙醇室温下在水中的溶解度大于溴乙烷 | |
| D. | 乙酸和甲酸甲酯互为同分异构体 |
20.下列说法正确的是( )
| A. | 瓦斯中甲烷和氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积比为1:2 | |
| B. | 欲配制1.00 L1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 | |
| C. | 22.4LN2和H2的混合气体中含NA个原子 | |
| D. | 3mol单质Fe完全转变为Fe3O4,得到8NA个电子 |
7.将固体NH4I置于密闭容器中,在一定温度下发生下列反应①NH4I(s)?NH3(g)+HI(g);②2HI(g)?H2(g)+I2(g).达到平衡时,c(H2)=1mol/L,c(HI)=3mol/L,则此温度下反应①的平衡常数为( )
| A. | 3 | B. | 9 | C. | 12 | D. | 15 |
4.下列微粒不具有氧化性的是( )
| A. | Cl2 | B. | Cl- | C. | H+ | D. | Fe3+ |
19. 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从下表中选出
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从下表中选出
正确选项 ( )
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从下表中选出
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从下表中选出正确选项 ( )
| 锥形瓶中的液 | 滴定管中的溶液 | 选用指示剂 | 选用滴定管 | |
| ① | 碱 | 酸 | 石蕊 | (乙) |
| ② | 酸 | 碱 | 酚酞 | (甲) |
| ③ | 碱 | 酸 | 酚酞 | (甲) |
| ④ | 酸 | 碱 | 酚酞 | (乙) |
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |