16.小明体检的血液化验单中,葡萄糖为5.9mmol/L.表示该体检指标的物理量是( )
| A. | 物质的量 | B. | 物质的量浓度 | C. | 质量分数 | D. | 摩尔质量 |
15.1mol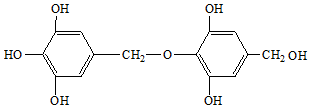 与足量的溴水共热,充分反应后,最多可消耗溴的物质的量是( )
与足量的溴水共热,充分反应后,最多可消耗溴的物质的量是( )
 与足量的溴水共热,充分反应后,最多可消耗溴的物质的量是( )
与足量的溴水共热,充分反应后,最多可消耗溴的物质的量是( )| A. | 3 mol | B. | 4 mol | C. | 5 mol | D. | 2 mol |
13.碱性电池具有容量大,放电电流大的特点,因而得到广泛的应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn+2MnO2+2H2O═Zn(OH)2+2MnOOH,下列说法不正确的是( )
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
12.某微粒用符号${\;}_{Z}^{A}$Mn+表示,下列关于该微粒的叙述中正确的是( )
| A. | 所含质子数为(A-n) | B. | 所含中子数为Z | ||
| C. | 所含电子数为(Z+n) | D. | 中子数-电子数=A-2Z+n |
11.类推是中学化学中重要的思维方法.下列类推结论正确的是( )
| A. | SiH4的沸点高于CH4,推测HCl的沸点高于HF | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
10.下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等 | |
| C. | 在标准状况下,22.4 L CH4与18 g H2O所含有电子数均为10NA | |
| D. | CO和N2为等电子体,22.4 L的CO气体与1 mol N2所含的电子数相等 |
9.硝酸生产中,500℃时,NH3和O2可能发生如下反应:
①4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g);△H=-907.2kJ•mol-1 K=1.1×1026
②4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g);△H=-1104.9kJ•mol-1 K=4.4×1028
③4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g);△H=-1269.2kJ•mol-1K=7.1×1034
下列说法正确的是( )
①4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g);△H=-907.2kJ•mol-1 K=1.1×1026
②4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g);△H=-1104.9kJ•mol-1 K=4.4×1028
③4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g);△H=-1269.2kJ•mol-1K=7.1×1034
下列说法正确的是( )
| A. | 增大压强,则反应的②K不变,反应①和③的K减小 | |
| B. | 500℃时,2NH3(g)+2O2 (g)?N2O (g)+3H2O (g) K=2.2×1028 | |
| C. | 500℃时,N2 (g)+O2 (g)=2NO (g)△H=+181 kJ•mol-1 | |
| D. | 500℃时,2 mol NH3 与2.5 mol O2混合发生反应①,可放出热量453.6 kJ |
8.下列说法中,错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 人体运动所消耗的能量与化学反应无关 | |
| C. | 在多能源时期,氢能、生物质能等的核心仍然是化学反应 | |
| D. | 核能、太阳能的利用取决于新型材料的合成与开发 |
7.已知,反应①:I2(aq)+I-(aq)?I3-(aq)△H1;
反应②:I3-(aq)?I2(aq)+I-(aq)△H2;
反应①的化学平衡常数K1与温度的关系如表:
请回答:
(1)若反应②的化学平衡常数为K2,在相同温度下,K1•K2=1.
(2)上述反应①的△H1<0(填“>”、“=”、“<”);若升高温度,则I2的溶解速率会加快(填“加快”、“减慢”或“不变”).
(3)能判断反应①已达到平衡的依据是BC
A.容器中的压强不再改变 B.溶液的颜色不再改变
C.I-浓度不再变化 D.正逆反应速率均为0
(4)某温度下,反应①的化学平衡常数为800.在该温度下,向甲、乙、丙三个容器中分别加入I2和I-,这两种物质的起始浓度如下:
反应速率最快的是丙(填“甲”、“乙”或“丙”),平衡时I2的转化率最大的是甲(填“甲”、“乙”或“丙”).
0 159841 159849 159855 159859 159865 159867 159871 159877 159879 159885 159891 159895 159897 159901 159907 159909 159915 159919 159921 159925 159927 159931 159933 159935 159936 159937 159939 159940 159941 159943 159945 159949 159951 159955 159957 159961 159967 159969 159975 159979 159981 159985 159991 159997 159999 160005 160009 160011 160017 160021 160027 160035 203614
反应②:I3-(aq)?I2(aq)+I-(aq)△H2;
反应①的化学平衡常数K1与温度的关系如表:
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K1 | 1100 | 841 | 680 | 533 | 409 |
(1)若反应②的化学平衡常数为K2,在相同温度下,K1•K2=1.
(2)上述反应①的△H1<0(填“>”、“=”、“<”);若升高温度,则I2的溶解速率会加快(填“加快”、“减慢”或“不变”).
(3)能判断反应①已达到平衡的依据是BC
A.容器中的压强不再改变 B.溶液的颜色不再改变
C.I-浓度不再变化 D.正逆反应速率均为0
(4)某温度下,反应①的化学平衡常数为800.在该温度下,向甲、乙、丙三个容器中分别加入I2和I-,这两种物质的起始浓度如下:
| 起始浓度(mol/L) | 甲 | 乙 | 丙 |
| c(I2) | 0.1 | 0.2 | 0.2 |
| c(I-) | 0.2 | 0.1 | 0.2 |

 CH3COOCH2CH3+H2O;反应类型酯化反应.
CH3COOCH2CH3+H2O;反应类型酯化反应.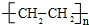 ;反应类型加聚反应.
;反应类型加聚反应.