1.在下述条件下,一定能大量共存的离子组是( )
| A. | 无色透明的水溶液中:K+、Ba2+、Cu2+、I- | |
| B. | 含有大量H+的水溶液中:NH4+、Fe2+、SO42-、MnO4- | |
| C. | c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br- | |
| D. | 强碱性溶液中:Cl-、SO32-、HSO3-、Na+ |
19.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
I.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:
Cr2O${\;}_{7}^{2-}$$→_{适量FeSO_{4}溶液}^{①H_{2}SO_{4}溶液}$Cr3+$\stackrel{③调节pH}{→}$Cr(OH)3$\stackrel{③加热}{→}$Cr2O3
有关离子完全沉淀的pH如表:
(1)写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O.
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
II.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:氯化钠是强电解质,增强溶液导电性.
I.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:
Cr2O${\;}_{7}^{2-}$$→_{适量FeSO_{4}溶液}^{①H_{2}SO_{4}溶液}$Cr3+$\stackrel{③调节pH}{→}$Cr(OH)3$\stackrel{③加热}{→}$Cr2O3
有关离子完全沉淀的pH如表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
II.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:氯化钠是强电解质,增强溶液导电性.
18.生产、生活离不开化学.下列说法中不正确的是( )
| A. | 高纯硅是工业上制造光导纤维的主要原料 | |
| B. | 开发和推广新能源汽车是实现低碳生活的途径之一 | |
| C. | 寻找高效催化剂,利用太阳能分解水是制取氢气的较理想方法 | |
| D. | 不需要通过化学反应就能从海水中获得淡水 |
17.下列关于有机物的叙述正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 乙酸和乙酸乙酯互为同分异构体 | |
| C. | 油脂和纤维素都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
16.下列离子方程式正确的是( )
| A. | 少量金属钠投入水中:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 60 mL 1 mol/L纯碱溶液与20 mL 2 mol/L胆矾溶液混合(无气体放出):3CO32-+2Cu2++2H2O=2HCO3-+Cu2(OH)2CO3↓ | |
| C. | 向H2O中投入少量Na218O2固体:2H2O+2Na218O2=4Na++418OH-+O2↑ | |
| D. | 向碳酸氢钙溶液中加入少量KOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
15.在常温下,水电离的c (H+)=1×10-13 mol•L-1的无色溶液中一定能大量共存的离子组是( )
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、Cl-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、NO3- | D. | Na+、Ca2+、Cl-、AlO2- |
14.下列有关有机化合物的说法正确的是( )
| A. | 聚乙烯可以使溴水褪色 | |
| B. | 乙烷与氯气发生取代反应,产物共有7种 | |
| C. | 煤中含有苯、甲苯和二甲苯 | |
| D. | 乙酸和油脂都能与NaOH溶液反应 |
13.下列有关化学用语使用正确的是( )
0 159466 159474 159480 159484 159490 159492 159496 159502 159504 159510 159516 159520 159522 159526 159532 159534 159540 159544 159546 159550 159552 159556 159558 159560 159561 159562 159564 159565 159566 159568 159570 159574 159576 159580 159582 159586 159592 159594 159600 159604 159606 159610 159616 159622 159624 159630 159634 159636 159642 159646 159652 159660 203614
| A. | CO2的电子式: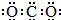 | |
| B. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S | |
| C. | 甲酸钠的分子式:CHO2Na | |
| D. | 乙烯的比例模型: |