题目内容
20.用18mol/L硫酸配制100mL 1.0mol/L硫酸.若实验仪器有:A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容量瓶、E.10mL量筒、F.胶头滴管、G.50mL烧杯、H.100mL容量瓶.实验时选用仪器的先后顺序是AFGCHF(填写编号).分析 先根据稀释前后溶质的物质的量不变,计算出浓溶液的体积,选取合适的量筒,再根据配制一定物质的量浓度的溶液需要量取、溶解、移液、洗涤、定容、摇匀等操作解答.
解答 解:配制1mol/L的稀硫酸100mL,需要浓硫酸的体积为V═$\frac{1mol/L×0.1L}{18mol/L}$=0.0125L=12.5mL,应选择100ml量筒,因配制一定物质的量浓度的溶液需要量取、稀释、移液、洗涤、定容、摇匀等操作,所以正确顺序为AFGCHF.
故答案为:AFGCHF.
点评 本题主要考查了配制一定物质的量浓度溶液的操作步骤和使用仪器,难度不大,应注意的是溶液稀释定律的有关利用和计算.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
11.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶 液 |
| A | 通入CO2,溶液变浑浊.再升温至65℃以上,溶液变澄清 | C6H5ONa溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失.再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失.再加热溶液,又变浑浊 | CaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.在常温下,水电离的c (H+)=1×10-13 mol•L-1的无色溶液中一定能大量共存的离子组是( )
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、Cl-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、NO3- | D. | Na+、Ca2+、Cl-、AlO2- |
5.在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀HCl,完全反应后,离子数目几乎没有改变的是( )
| A. | Fe2+ | B. | Fe3+ | C. | Al3+ | D. | NH4+ |
12.从下列实验事实所得出的相应结论正确的是( )
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷可自燃而氮气需在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
| A. | ②③⑤ | B. | ①②③ | C. | ③④⑤ | D. | ①③⑤ |
9.如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是
 ( )
( )
 ( )
( )| A. | W的氢化物比R的氢化物稳定 | |
| B. | T的最高价氧化物水化物可能为强碱 | |
| C. | Q的原子半径比T的小 | |
| D. | W和Q的原子序数相差10 |
19.下列反应离子方程式错误的是( )
| A. | 少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=2HClO+SO32- | |
| B. | 碳酸钙中滴入醋酸溶液:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ | |
| C. | 碳酸氢镁溶液中加入过量的澄清石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O | |
| D. | 硫酸亚铁溶液中加过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
 ③C的化学式为C15H13NO4,-Bn含苯环但不含甲基.
③C的化学式为C15H13NO4,-Bn含苯环但不含甲基.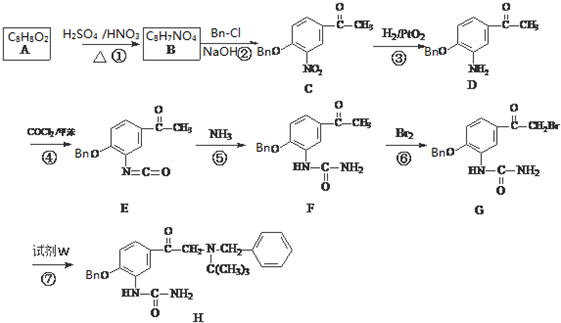
 W
W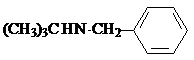 .
.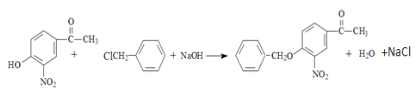 .
.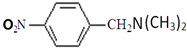 (无机试剂任用)
(无机试剂任用)