12.下列实验能获得成功的是( )
| A. | 氯乙烷与NaOH溶液共热,在反应后的溶液中加入AgNO3溶液检验Cl- | |
| B. | 在淀粉加入硫酸加热水解后的溶液中,直接加入银氨溶液,水浴加热,检验葡萄糖的生成 | |
| C. | 1 mol•L-1 CuSO4溶液2 mL和0.5 mol•L-1 NaOH溶液4 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸观察沉淀的颜色 | |
| D. | 除去乙烯中杂质气体:将实验室制得的乙烯气体通入NaOH 溶液 |
11.瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是( )
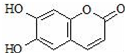

| A. | 与稀H2SO4混合加热不反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol 瑞香素最多能与3mol Br2发生反应 | |
| D. | 1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 2mol |
10.下列反应中,不属于取代反应的是( )
| A. | 乙醇与氧气反应生成醛 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 乙醇与浓硫酸加热到140℃ | |
| D. | 乙酸乙酯与稀硫酸共热 |
9.下列有关化学用语或名称表达正确的是( )
| A. | 亚硫酸的电离方程式:H2SO3?2H++SO32- | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式: | |
| D. |  互为同系物 互为同系物 |
8.已知锌与稀盐酸反应放热.某学生为了探究反应过程中的速率变化,用排水集气法收集反应放出的氢气.所用稀盐酸浓度有1.00mol•L-1、2.00mol•L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30s~40s范围内盐酸的平均反应速率ν(HCl)=0.056mol•L-1•s-1.(忽略溶液体积变化,不需要写出计算过程).
②反应速率最大的时间段(即0s~10s、10s~20s、20s~30s、30s~40s…)为40s~50s,可能原因是反应放热.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率:
A.氨水 B.CuCl2溶液 C.NaCl溶液 D.KNO3溶液
你认为他上述做法中可行的是C(填相应字母);
(4)另有某温度时,在2L容器中X、Y、Z物质的量随时间的变化关系曲线如下图1所示,该反应的化学方程式为:3X+Y?2Z.
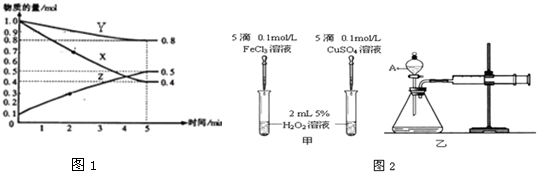
(5)在化学反应速率的学习中,某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,分别设计了如下图甲、乙所示的实验.请回答相关问题:
①定性分析:如图2甲可通过观察生成气泡的快慢判断,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子不同造成的干扰.
②定量分析:如图2乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,实验中需要测量的数据是收集40mL气体所需要的时间.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 | T/K | 锌规格 | 盐酸浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究锌规格(粗、细)对该反应速率的影响. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 时间(s) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积 (mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(即0s~10s、10s~20s、20s~30s、30s~40s…)为40s~50s,可能原因是反应放热.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率:
A.氨水 B.CuCl2溶液 C.NaCl溶液 D.KNO3溶液
你认为他上述做法中可行的是C(填相应字母);
(4)另有某温度时,在2L容器中X、Y、Z物质的量随时间的变化关系曲线如下图1所示,该反应的化学方程式为:3X+Y?2Z.

(5)在化学反应速率的学习中,某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,分别设计了如下图甲、乙所示的实验.请回答相关问题:
①定性分析:如图2甲可通过观察生成气泡的快慢判断,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子不同造成的干扰.
②定量分析:如图2乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,实验中需要测量的数据是收集40mL气体所需要的时间.
7.化学与生产,生活密切相关,下列有关说法中正确的是( )
| A. | 玻璃、水泥、水晶都是硅酸盐制品 | |
| B. | 将秸秆焚烧可得富含钾肥的草木灰,焚烧是一种较为理想的秸秆处理办法 | |
| C. | 石油的分馏和煤的气化、液化,涉及的都是物理变化 | |
| D. | 纤维素不能被人体消化吸收,但能促进肠道的蠕动,对人体有益 |
5.向一固定体积的密闭容器中通入a mol N2O4气体,在密闭容器内发生反应:N2O4(g)?2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
4.一定温度下,在一容积不变的密闭容器中,充入一定量HI气体,发生如下可逆反应:2HI(g)?H2(g)+I2(g)△H>0.下列说法正确的是( )
| A. | 若每消耗2n mol HI的同时生成n mol H2,表明该反应已达平衡 | |
| B. | 容器内的压强不发生变化,表明该反应已达平衡 | |
| C. | 平衡时,若其他条件不变,再充入一定量HI,重新达平衡后,I2的百分含量增大 | |
| D. | 平衡时,若其他条件不变,升高温度,混合气体的颜色加深 |
3.浓度均为0.01mol/L硫氰化钾与氯化铁溶液各100mL在一定条件下反应:
3KSCN+FeCl3?Fe(SCN)3+3KCL
达到平衡后向混合溶液加入5g下列固体(溶液体积变化忽略不计),不影响平衡的是( )
0 157428 157436 157442 157446 157452 157454 157458 157464 157466 157472 157478 157482 157484 157488 157494 157496 157502 157506 157508 157512 157514 157518 157520 157522 157523 157524 157526 157527 157528 157530 157532 157536 157538 157542 157544 157548 157554 157556 157562 157566 157568 157572 157578 157584 157586 157592 157596 157598 157604 157608 157614 157622 203614
3KSCN+FeCl3?Fe(SCN)3+3KCL
达到平衡后向混合溶液加入5g下列固体(溶液体积变化忽略不计),不影响平衡的是( )
| A. | 氯化铁 | B. | 氯化钾 | C. | 硫氰化钾 | D. | 氢氧化钠 |