题目内容
6.现有两瓶失去标签的Na2CO3和NaHCO3无色的饱和溶液,请提出简便的鉴别方法,其中不合理的是( )①用干燥的pH试纸检验,pH大的是Na2CO3
②取同量的溶液于两支试管中,各滴入酚酞试液,红色较深的是Na2CO3
③取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO3
④取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3
⑤取同量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3.
| A. | ①② | B. | ③ | C. | ④⑤ | D. | ②⑤ |
分析 ①等浓度时碳酸钠的水解程度大;
②等浓度时碳酸钠的水解程度大,碱性强;
③溶液加热不分解;
④与盐酸反应,碳酸氢钠反应快;
⑤碳酸钠与氯化钡反应,而碳酸氢钠不反应.
解答 解:①碳酸钠、碳酸氢钠都是强碱弱酸盐水解呈碱性,同温度相同物质的量浓度碳酸钠、碳酸氢钠溶液中,Na2CO3水解程度大于NaHCO3,所以Na2CO3溶液中氢氧根离子浓度大,pH大,故正确;
②Na2CO3较NaHCO3水解程度大,分别滴加酚酞试液,红色较深的是Na2CO3溶液,故正确;
③取同量的溶液于两支试管中,加热,均没有气体生成,故错误;
④取同量的溶液于两支试管中,逐滴加入稀盐酸,碳酸氢钠反应快,开始就有气体放出的是NaHCO3,故正确;
⑤取同量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3,而碳酸氢钠与氯化钡不反应,故正确;
故选B.
点评 本题考查Na2CO3和NaHCO3性质的异同,为高频考点,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
16.硅被誉为无机非金属材料的主角,硅单质可用来制作( )
| A. | 陶瓷餐具 | B. | 石英表 | C. | 计算机芯片 | D. | 光导纤维 |
14.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 22.4L氮气中含NA个氮原子 | |
| B. | 在标准状况下,1mol水的体积约为22.4L | |
| C. | 0.3 mol•L-1Na2SO4溶液中含0.6NA个Na+ | |
| D. | 18 g水中所含的氢原子数目为2NA |
1.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA个 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| C. | 17.6 g丙烷中所含的极性共价键为4NA个 | |
| D. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA |
11.瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是( )
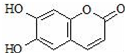

| A. | 与稀H2SO4混合加热不反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol 瑞香素最多能与3mol Br2发生反应 | |
| D. | 1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 2mol |
18. 如图所示,两个连通容器用活塞分开,左右两室体积相同,左室充入一定里NO,右室充入一定量O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应,下列判断正确的是(不考虑NO2转化为N2O4)( )
如图所示,两个连通容器用活塞分开,左右两室体积相同,左室充入一定里NO,右室充入一定量O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应,下列判断正确的是(不考虑NO2转化为N2O4)( )
 如图所示,两个连通容器用活塞分开,左右两室体积相同,左室充入一定里NO,右室充入一定量O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应,下列判断正确的是(不考虑NO2转化为N2O4)( )
如图所示,两个连通容器用活塞分开,左右两室体积相同,左室充入一定里NO,右室充入一定量O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应,下列判断正确的是(不考虑NO2转化为N2O4)( )| A. | 反应前后左室的压强相同 | |
| B. | 开始时左右两室中的分子数相同 | |
| C. | 反应后容器内的密度与反应前的相同 | |
| D. | 反应后容器内无O2存在 |
15.与CH2═CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A. | CH≡CH→CH2═CHCN | B. | C2H5Cl→CH2═CH2 | ||
| C. | C6H6→C6H6-NO2 | D. | CH3COOH→CH3COOC2H5 |
16.下列一组粒子的中心原子杂化类型相同,分子或原子的键角不相等的是( )
| A. | SiCl4、金刚石 | B. | H2S、NF3 | C. | CH2═CHCl、环已烷 | D. | C6H6(苯)、CH3C≡CH |