10.下列说法中错误的是( )
| A. | 干冰与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 | |
| B. | 白磷(P4)分子是正四面体结构,故分子中的键角为1090281 | |
| C. | CsCl晶体中每个Cs+周围紧邻的Cl-和每个Cl-周围紧邻的Cs+个数相等 | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
4.下列叙述正确的是( )
| A. | C15H31COOH和C17H35COOH是同系物 | |
| B. | 结构不同,性质相同,化学式相同的物质互称同分异构体 | |
| C. | 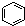 和 和 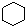 均是芳香烃, 均是芳香烃,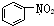 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 | |
| D. | 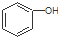 和 和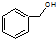 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
1.现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)已知B2A4是一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,能很好地混溶于水,遇卤素、过氧化氢等强氧化剂作用能自燃.B2A4属于极性分子(填“极性”或“非极性”),B2A4分子中B原子轨道的杂化形式为sp3.写出B2A4的电子式: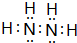 .
.
(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.
(4)分析DE3分子的空间构型为三角锥形.
(5)G位于第Ⅷ族d区,该元素的核外电子排布式为1s22s22p63s23p63d74s2.
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂.
GE2+xH2O=GE2•xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2•xH2O 119g.
①水合物中x=6.
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为[CoCl(H2O)5]Cl•H2O.
0 156457 156465 156471 156475 156481 156483 156487 156493 156495 156501 156507 156511 156513 156517 156523 156525 156531 156535 156537 156541 156543 156547 156549 156551 156552 156553 156555 156556 156557 156559 156561 156565 156567 156571 156573 156577 156583 156585 156591 156595 156597 156601 156607 156613 156615 156621 156625 156627 156633 156637 156643 156651 203614
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中未成对电子最多的元素 |
| G的3d能级只含有2对成对电子 |
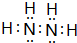 .
.(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.(4)分析DE3分子的空间构型为三角锥形.
(5)G位于第Ⅷ族d区,该元素的核外电子排布式为1s22s22p63s23p63d74s2.
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂.
GE2+xH2O=GE2•xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2•xH2O 119g.
①水合物中x=6.
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为[CoCl(H2O)5]Cl•H2O.
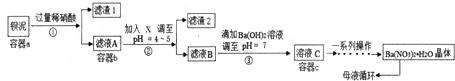
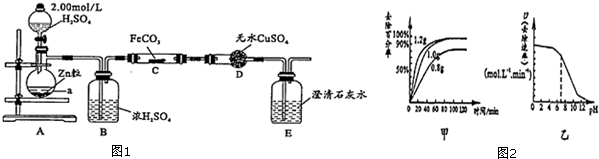
 水合肼(N2H4•H2O)为无色透明的油状液体,沸点为118.5℃,熔点为-40℃.具有强碱性,在空气中可吸收CO2,产生烟雾.水合肼是一种强还原剂,能与卤素单质、HNO3、KMnO4等激烈反应.水合肼可用含NaOH的NaClO溶液氧化尿索[CO(NH2)2]溶液制得.实验室模拟水合肼的制备装置如图所示(夹持及加热装置已省略).请回答下列问题:
水合肼(N2H4•H2O)为无色透明的油状液体,沸点为118.5℃,熔点为-40℃.具有强碱性,在空气中可吸收CO2,产生烟雾.水合肼是一种强还原剂,能与卤素单质、HNO3、KMnO4等激烈反应.水合肼可用含NaOH的NaClO溶液氧化尿索[CO(NH2)2]溶液制得.实验室模拟水合肼的制备装置如图所示(夹持及加热装置已省略).请回答下列问题: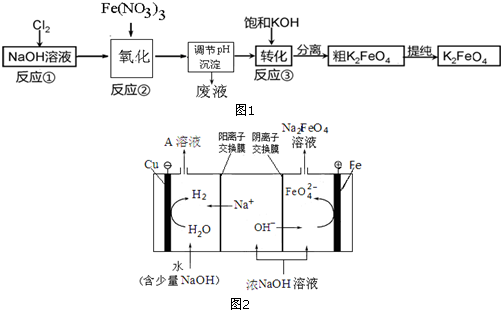
 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数位次递增.B原子的p轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的是.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子 化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体. 请根据以上信息,回答下列问题:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数位次递增.B原子的p轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的是.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子 化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体. 请根据以上信息,回答下列问题: