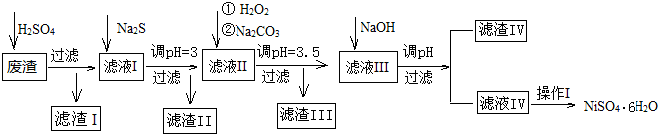
18.金属镍在电池和电镀等工业上具有广泛的用途,可镍也具有很强的毒性,若不进行回收处理,将对环境造成很大的影响,以下是以电镀废渣为原料获得NiSO4•6H2O的过程,已知,废渣中除含金属镍外,主要含有:Cu、Zn、Fe、Mg等元素的化合物.
部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表.
(1)往废渣中加H2SO4酸浸,提高酸浸效率的方法有搅拌、升温、适当增加硫酸浓度、废渣粉碎等(至少写出2点)
(2)加Na2S同时调溶液的pH为3,目的是除去铜、锌等杂质,则往滤液Ⅱ中加入H2O2的反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)操作Ⅰ包括以下过程:冷却、结晶、过滤、洗涤、干燥.该洗涤过程不能用水洗涤,应该用酒精洗涤,目的是既能洗涤沉淀表面残余的溶液又有利晶体的干燥并减少NiSO4﹒6H2O晶体的损失.干燥有低温干燥和高温干燥,能否用高温干燥否,理由是温度过高会使NiSO4﹒6H2O晶体失去部分或全部结晶水.
(4)滤液Ⅲ中加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,若向含有Mg2+、Al3+的溶液中滴加NaOH溶液,常温下当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Al3+)=2.5×1013.{已知:25℃时,KSP[Mg(OH)2]=5.0×10-14;KSP[Al(OH)3]=2.0×10-33}.

部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | CuS | ZnS | FeS | NiS | Al(OH)3 | Mg(OH)2 | Ni(OH)2 |
| pH | 3.2 | 9.7 | ≥-0.42 | ≥2.5 | ≥7 | ≥7.5 | ≥5 | ≥8 | ≥8.5 |
(2)加Na2S同时调溶液的pH为3,目的是除去铜、锌等杂质,则往滤液Ⅱ中加入H2O2的反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)操作Ⅰ包括以下过程:冷却、结晶、过滤、洗涤、干燥.该洗涤过程不能用水洗涤,应该用酒精洗涤,目的是既能洗涤沉淀表面残余的溶液又有利晶体的干燥并减少NiSO4﹒6H2O晶体的损失.干燥有低温干燥和高温干燥,能否用高温干燥否,理由是温度过高会使NiSO4﹒6H2O晶体失去部分或全部结晶水.
(4)滤液Ⅲ中加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,若向含有Mg2+、Al3+的溶液中滴加NaOH溶液,常温下当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Al3+)=2.5×1013.{已知:25℃时,KSP[Mg(OH)2]=5.0×10-14;KSP[Al(OH)3]=2.0×10-33}.
17.下列实验操作能达到预期实验目的是( )
| 实验目的 | 实验操作 |
| A.证明Fe3+与SO2发生了氧化还原反应 | 将过量SO2通入FeCl3溶液中,然后将反应液加入酸性高锰酸钾溶液中,发现高锰酸钾溶液褪色. |
| B.除去CH3COOC2H5中的乙醇 | 加入适量CH3COOH,加热 |
| C.鉴别等浓度的Na2CO3溶液和NaHCO3溶液 | 分别向未知的溶液中滴加同浓度的盐酸,观察 现象 |
| D.比较H2CO3、HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液 的pH值,比较pH大小 |
| A. | A | B. | B | C. | C | D. | D |
16.有A.B.C.D.E五种短周期主族元素,原子序数依次增大,其中A是宇宙中含量最高的元素,其原子核中无中子,B,D同主族,且B、D最外层电子数之和与A、C的质子数之和相等.C是同周期中原子半径最大的主族元素,下列说法不正确的是( )
| A. | E的单质不具有漂白能力 | |
| B. | A2D与DB2可发生氧化还原反应,氧化产物与还原产物的质量比为2:1 | |
| C. | A2D的还原性弱于AE的还原性 | |
| D. | B与C形成的两种离子化合物中,阴、阳离子个数比相等且所含化学键类型不完全相同 |
15.25℃时,有c(CH3COOH)+c(CH3COO-)=0.2mol.L-1的一组醋酸与醋酸钾的混合溶液,溶液中的c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关说法正确的是( )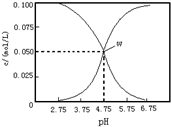

| A. | 该温度下醋酸的电离平衡常数为ka=10-4.75 | |
| B. | pH=6的溶液中,c(K+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L | |
| C. | pH=3.75的溶液中c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | 向W点所示溶液中通入0.1molHCl气体(溶液体积可以忽略不计)c(H+)=c(OH-)+c(CH3COOH) |
14.下列说法或者方程式正确的是( )
| A. | 使酚酞变红的溶液中,这些离子不可大量共存:Cl-,S2-,SO32-,K+ | |
| B. | 向CH3COOH溶液中滴加NaOH的过程中,计算式$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$的值始终不变 | |
| C. | 苯酚钠溶液中通入少量CO2,发生反应:2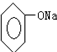 +H2O+CO2→2 +H2O+CO2→2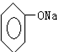 +Na2CO3 +Na2CO3 | |
| D. | 硝酸亚铁溶液中滴入盐酸的离子反应方程式为:3Fe2++4H++NO3-═3Fe3++NO+2H2O |
13.若生产者固定的太阳能等于消费者呼吸散失的能量,则该自然生态系统处于稳态化学与生活、生产联系紧密,下列说法不正确的是( )
| A. | 过氧化钠常用于远途运输鱼苗的供氧 | |
| B. | 侯式制碱法的工艺过程中应用了物质的溶解性差异 | |
| C. | 加工后具有吸水性的植物纤维可用作食品干燥剂 | |
| D. | 使用含有钙离子浓度较大的地下水洗衣服,肥皂的去污能力减弱 |
11. 电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液滴定10.00mL浓度均为0.100mol•L-1 的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液滴定10.00mL浓度均为0.100mol•L-1 的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
 电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液滴定10.00mL浓度均为0.100mol•L-1 的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液滴定10.00mL浓度均为0.100mol•L-1 的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )| A. | 曲线①代表滴定HCl溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1mol•L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水的电离程度:C<B<A | |
| D. | D点溶液中:c(Cl-)=2c(OH-)-2c(H+) |
10.由一种阳离子与两种酸根离子组成的盐称为混盐.混盐Na4S2O3,在酸性条件下可以产生S.下列关于混盐
Na4S2O3的有关判断不正确的是( )
0 154793 154801 154807 154811 154817 154819 154823 154829 154831 154837 154843 154847 154849 154853 154859 154861 154867 154871 154873 154877 154879 154883 154885 154887 154888 154889 154891 154892 154893 154895 154897 154901 154903 154907 154909 154913 154919 154921 154927 154931 154933 154937 154943 154949 154951 154957 154961 154963 154969 154973 154979 154987 203614
Na4S2O3的有关判断不正确的是( )
| A. | 该混盐的水溶液呈碱性 | |
| B. | 该混盐溶液中加人BaCl2溶液,可以生成白色沉淀 | |
| C. | 该混盐与稀硫酸反应产生1mol S时转移2NA个电子 | |
| D. | 该混盐中的硫元素的化合价为-2和+4 |