14.25℃时有关弱酸的电离平衡常数关系为:Ki(CH3COOH)>Ki1(H2CO3)>Ki(HCN)>Ki2(H2CO3).在冰醋酸中逐滴加水,溶液导电性和加水体积的关系如图所示.下列说法正确的是( )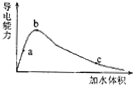

| A. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) | |
| B. | 冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| C. | 混合溶液中含有等物质的量的Na2CO3和NaHCO3,则一定存在c(Na+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| D. | a mol/LHCN溶液与b mol/LNaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则b一定大于a |
12.有aXn+ 和bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A. | b-a=n+m | B. | a-b=n-m | C. | 质子数Y>X | D. | 核电荷数Y<X |
11.下列指定溶液中一定能大量共存的离子组是( )
| A. | pH=1的溶液中:NH4+、Na+、Fe3+、SO42- | |
| B. | 中性溶液中:K+、Fe3+、Cl-、SO42- | |
| C. | AlO2一的浓度为0.1 mol/L的溶液中:K+、Na+、HCO3-、SO42- | |
| D. | Na2S溶液中:SO42-、K+、Cu2+、Cl- |
10. 室温下,将0.10mol•L-1盐酸滴入20.00mL 0.10mol•L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )
室温下,将0.10mol•L-1盐酸滴入20.00mL 0.10mol•L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )
 室温下,将0.10mol•L-1盐酸滴入20.00mL 0.10mol•L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )
室温下,将0.10mol•L-1盐酸滴入20.00mL 0.10mol•L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示.已知:pOH=-lg c(OH-),下列说法正确的是( )| A. | M点所示溶液中c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| B. | N点所示溶液中c(NH4+)>c(Cl-) | |
| C. | Q点消耗盐酸的体积等于氨水的体积 | |
| D. | M点和N点所示溶液中水的电离程度相同 |
9.下列实验装置、试剂选用或操作正确的是( )
| A. | 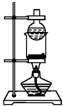 分离NaCl、I2混合物 | B. | 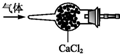 干燥CO2气体 | ||
| C. | 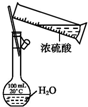 稀释浓硫酸 | D. | 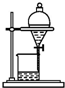 分离溴、CCl4混合物 |
6.下列说法正确的是( )
| A. | BaSO4在熔化状态下导电的本质原因是其中存在自由移动的离子 | |
| B. | 氯化银难溶于水,故其水溶液不导电 | |
| C. | 液态HCl中含有自由移动的Cl- | |
| D. | 电离是电解质在通电的作用下离解成自由移动的离子的过程 |
5.在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+I2(g)?2HI(g).已知起始时加入1mol H2和2mol I2(g),当达到平衡时H2的体积分数为φ.下列四种情况分别投入上述容器,且始终保持原温度,平衡时H2的体积分数也为φ的是( )
0 154721 154729 154735 154739 154745 154747 154751 154757 154759 154765 154771 154775 154777 154781 154787 154789 154795 154799 154801 154805 154807 154811 154813 154815 154816 154817 154819 154820 154821 154823 154825 154829 154831 154835 154837 154841 154847 154849 154855 154859 154861 154865 154871 154877 154879 154885 154889 154891 154897 154901 154907 154915 203614
| A. | 2 mol H2(g)和1 mol I2(g) | B. | 3 mol HI(g) | ||
| C. | 2 mol H2(g)和2 mol I2(g) | D. | 1 mol I2(g)和2 mol HI(g) |
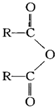 $\stackrel{H_{2}O}{→}$2RCOOH(其中R是烃基)
$\stackrel{H_{2}O}{→}$2RCOOH(其中R是烃基)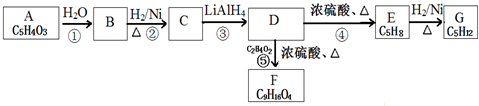
 ,CH2=C(CH3)CH=CH2.
,CH2=C(CH3)CH=CH2.
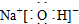 .
.