3.含硫化合物在自然界中广泛存在,部分循环关系如下:
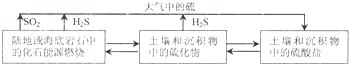
(1)已知:
2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)△H=-1036.46kj.mol-1
S(s)+O2(g)═SO2(g)△H=-297.04kJ.mol-1
写出H2S(g)与O2(g)反应产生S(s)和H2O(g)的热化学方程式2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-442.38kJ.mol-1.
(2)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS,慢慢转变为铜蓝(CuS),用离子方程式,从沉淀溶解平衡的角度表示由ZnS转变为CuS的过程ZnS(S)+Cu2+(aq)?Zn2+(aq)+CuS(S).
(3)某酸性FeSO4溶液中含有少量的SnSO4,为得到纯净的硫酸亚铁晶体(FeSO4•xH2O),可向溶液中通入H2S气体至饱和,然后用硫酸酸化至Ph=2,过滤后,将所得滤液蒸发浓缩,冷却结晶,过滤洗涤,得到硫酸亚铁晶体.查阅资料,得到相关物质的有关数据如下表:
①通入H2S气体至饱和的目的是将溶液中的Sn2+转变为SnS而除去;用硫酸酸化至pH=2的目的是防止Fe2+转化为FeS沉淀.
②在SnS、FeS共存的溶液中,若c(Sn2+)=1.0×10-9mol•L-1,则c(Fe2+)=6.3×10-2mol•L-1.
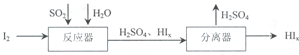
(4)SO2是大气污染物,若用KMnO4作脱硫剂,可使燃煤尾气中的SO2反应生成MnSO4,反应的离子方程式是2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+.SO2还可以按下列流程制备化工原料硫酸,反应器中发生反应的化学方程式是SO2+xI2+2H2O=H2SO4+2HIx.

(1)已知:
2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)△H=-1036.46kj.mol-1
S(s)+O2(g)═SO2(g)△H=-297.04kJ.mol-1
写出H2S(g)与O2(g)反应产生S(s)和H2O(g)的热化学方程式2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-442.38kJ.mol-1.
(2)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS,慢慢转变为铜蓝(CuS),用离子方程式,从沉淀溶解平衡的角度表示由ZnS转变为CuS的过程ZnS(S)+Cu2+(aq)?Zn2+(aq)+CuS(S).
(3)某酸性FeSO4溶液中含有少量的SnSO4,为得到纯净的硫酸亚铁晶体(FeSO4•xH2O),可向溶液中通入H2S气体至饱和,然后用硫酸酸化至Ph=2,过滤后,将所得滤液蒸发浓缩,冷却结晶,过滤洗涤,得到硫酸亚铁晶体.查阅资料,得到相关物质的有关数据如下表:
| 25℃ | 饱和H2S溶液 | FeS | SnS | |
| pH | 3.9 | 3.0(开始沉淀 | 5.5(沉淀完全) | 1.6(沉淀完全) |
| Ksp | 6.3×10-18 | 1.0×10-25 | ||
②在SnS、FeS共存的溶液中,若c(Sn2+)=1.0×10-9mol•L-1,则c(Fe2+)=6.3×10-2mol•L-1.
(4)SO2是大气污染物,若用KMnO4作脱硫剂,可使燃煤尾气中的SO2反应生成MnSO4,反应的离子方程式是2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+.SO2还可以按下列流程制备化工原料硫酸,反应器中发生反应的化学方程式是SO2+xI2+2H2O=H2SO4+2HIx.

2.一定量的Fe和Fe2O3的混合物投入250ml密度为1.065g.cm-3、物质的量浓度为2mol•L-1的HNO3溶液中,固体恰好完全溶解,生成Fe(NO3)2和1.12LNO(标况下,且假定HNO3还原产物仅此一种).向反应后的溶液中加入1mol•L-1NaOH溶液,使铁元素完全沉淀下来,下列说法正确的是( )
| A. | 混合物中含有0.05molFe元素 | |
| B. | 该硝酸溶液中溶质的质量分数是63% | |
| C. | 所加入NaOH溶液的体积最少是450mL | |
| D. | 反应中HNO3被氧化,生成氧化产物NO |
1. 将溶液 的c(H+)、c(OH-)之比取为AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃时,用0.01mol.L-1的氢氧化钠溶液滴定20ml相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )
将溶液 的c(H+)、c(OH-)之比取为AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃时,用0.01mol.L-1的氢氧化钠溶液滴定20ml相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )
 将溶液 的c(H+)、c(OH-)之比取为AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃时,用0.01mol.L-1的氢氧化钠溶液滴定20ml相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )
将溶液 的c(H+)、c(OH-)之比取为AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃时,用0.01mol.L-1的氢氧化钠溶液滴定20ml相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )| A. | A点时c(CH3COO-)>c(Na+) | |
| B. | 室温时0.01mol.L-1的醋酸溶液pH=6 | |
| C. | OA段溶液中均有:c(CH3COO-)>c(CH3COOH) | |
| D. | 若B点时加入NaOH溶液40mL,所得溶液中:c(CH3COO-)+2c(CH3COOH)=c(OH-)-c(H+) |
20.短周期元素X、Y、Z、W原子序数依次增大,Y、Z、W的最高价氧化物对应水化物间可两两反应生成盐和水;化合物YWX是漂白液的有效成分.下列说法正确的是( )
| A. | Z单质还原性大于Y单质 | |
| B. | X的氢化物沸点高于W的氢化物 | |
| C. | 仅含X、Y两元素的化合物均只含离子键 | |
| D. | 上述四种元素形成的简单离子中,X离子半径最小 |
19.下列说法不正确的是( )
| A. | 二甲苯和四甲苯均有三种 | |
| B. | 乙醇的酯化反应和酯的水解均属于取代反应 | |
| C. | 乙醇、乙酸均可与金属钠反应 | |
| D. | 石油裂解和油脂皂化均是由高分子物质生成小分子物质的过程 |
18.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24L乙醇分子所含的C-H键数为0.5NA | |
| B. | 3.2克O2和O3的混合气中含有的氧原子数目为0.2NA | |
| C. | 0.1mol•L-1的Al2(SO4)3溶液中,AL3+的数目小于0.2NA | |
| D. | 0.1molFe参加氧化还原反应,转移的电子数目一定是0.3NA |
17.下列说法正确的是( )
0 154706 154714 154720 154724 154730 154732 154736 154742 154744 154750 154756 154760 154762 154766 154772 154774 154780 154784 154786 154790 154792 154796 154798 154800 154801 154802 154804 154805 154806 154808 154810 154814 154816 154820 154822 154826 154832 154834 154840 154844 154846 154850 154856 154862 154864 154870 154874 154876 154882 154886 154892 154900 203614
| A. | 氯气与明矾处理水的原理完全相同 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 植物通过光合作用将二氧化碳转化为糖是太阳能转变成热能的过程 | |
| D. | 铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀 |

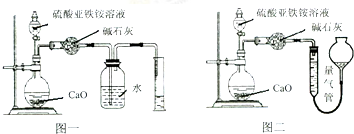
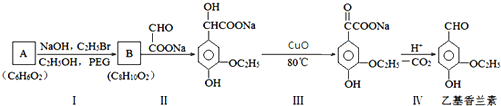
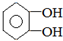 .
.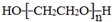 .若PEG的平均相对分子质量为17618,则其平均聚合度约为400.
.若PEG的平均相对分子质量为17618,则其平均聚合度约为400.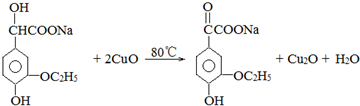 .
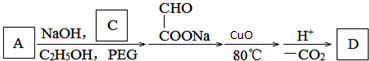
.
 .
.