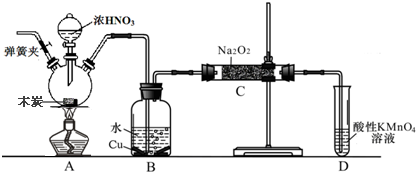
20. 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
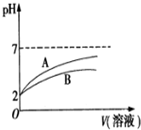
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
①根据表中数据判断t时刻此反应向正反应方向进行(选填“正”或“逆”).
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
| 物质 | Cl2 | TiCl4 | O2 |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
17.下列原子中未成对电子最多的是( )
| A. | C | B. | O | C. | N | D. | Cl |
16.下列反应中的氨与反应4NH3+5O2=4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3═2NaNH2+H2↑ | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 4NH3+6NO═5N2+6H2O | D. | HCl+NH3═NH4Cl |
15.下列离子方程式书写正确的是( )
| A. | AgNO3溶液中滴入少量的Na2S溶液 2Ag NO3+S2-=Ag2S↓+2NO3- | |
| B. | 过量CO2通入Ca(ClO)2溶液中 ClO-+CO2+H2O=HCO3-+HClO | |
| C. | 向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+=CO2↑+H2O | |
| D. | 向Ba(OH)2溶液中加入少量NaHCO3溶液 2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O |
14.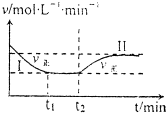 在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )
在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )
 在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )
在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )| A. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数:KⅠ<KⅡ | |
| B. | Ⅰ、Ⅱ两过程达到平衡时,NH3的体积分数:Ⅰ<Ⅱ | |
| C. | Ⅰ、Ⅱ两过程达到平衡的标志:气体密度不再发生变化 | |
| D. | t2时刻改变的条件可以是向密闭容器中加H2和N2混合气 |
13.有关氧化还原反应的下列说法中正确的是( )
| A. | 还原剂发生还原反应 | B. | 一定有氧元素参与反应 | ||
| C. | 一定有元素化合价升降 | D. | 氧化剂失去电子,化合价升高 |
12.已知相同温度下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
0 154671 154679 154685 154689 154695 154697 154701 154707 154709 154715 154721 154725 154727 154731 154737 154739 154745 154749 154751 154755 154757 154761 154763 154765 154766 154767 154769 154770 154771 154773 154775 154779 154781 154785 154787 154791 154797 154799 154805 154809 154811 154815 154821 154827 154829 154835 154839 154841 154847 154851 154857 154865 203614
| A. | 水的电离程度始终增大 | |
| B. | c(NH4+):c(NH3•H2O)始终减小 | |
| C. | c(CH3COOH)与c(CH3COO?)之和始终保持不变 | |
| D. | 当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-) |
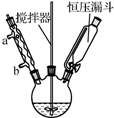 以香豆素3甲酸乙酯(
以香豆素3甲酸乙酯(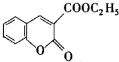 )为原料合成香豆素3甲酸(
)为原料合成香豆素3甲酸(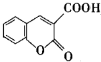 )的装置如图所示,实验步骤如下:
)的装置如图所示,实验步骤如下: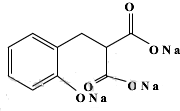 +C2H5OH+H2O.
+C2H5OH+H2O.