19.下列关于胶体的叙述中不正确的是( )
| A. | 丁达尔现象可用区别胶体与溶液 | |
| B. | 胶体不稳定,在一定条件下会发生聚沉 | |
| C. | 胶体粒子能通过半透膜,不能通过滤纸 | |
| D. | 溶液、胶体、浊液的根本区别是分散质粒子直径的大小 |
18.通过溶解、过滤、蒸发等操作,可以将下列各组固体混合物分离的是( )
| A. | 硝酸钠 氢氧化钠 | B. | 氧化铜 二氧化锰 | ||
| C. | 氯化钾 碳酸钙 | D. | 硫酸铜 氢氧化钠 |
17.下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A. | Ag+、NO3-、Cl-、K+ | B. | K+、Ba2+、OH-、SO42- | ||
| C. | H+、NO3-、Fe2+、Na+ | D. | Cu2+、NH4+、Cl-、OH- |
16.将下列各组物质按酸、碱、盐分类顺序排列,其中正确的是( )
| A. | 硫酸、纯碱、漂白粉 | B. | 硫酸、烧碱、小苏打 | ||
| C. | 硫酸氢钠、生石灰、醋酸钠 | D. | 磷酸、熟石灰、苛性钠 |
15.同温同压下,相同质量的下列气体中,体积最大的是( )
| A. | N2 | B. | SO2 | C. | Cl2 | D. | CO2 |
14.下列氢化物中最稳定的是( )
| A. | HF | B. | HCl | C. | HB | D. | HI |
13.下列物质中,属于纯净物的是( )
0 154591 154599 154605 154609 154615 154617 154621 154627 154629 154635 154641 154645 154647 154651 154657 154659 154665 154669 154671 154675 154677 154681 154683 154685 154686 154687 154689 154690 154691 154693 154695 154699 154701 154705 154707 154711 154717 154719 154725 154729 154731 154735 154741 154747 154749 154755 154759 154761 154767 154771 154777 154785 203614
| A. | 水泥 | B. | 漂白粉 | C. | 胆矾 | D. | 氯水 |
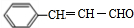 .
.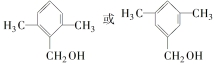 .
.