题目内容
13.下列物质中,属于纯净物的是( )| A. | 水泥 | B. | 漂白粉 | C. | 胆矾 | D. | 氯水 |
分析 纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;据此结合常见物质的组成成分逐项分析即可.
解答 解:A.水泥是硅酸盐材料,是混合物,故A错误;
B.漂白粉主要成分为次氯酸钙和氯化钙,是混合物,故B错误;
C.胆矾是结晶水合物是化合物,化学式为CuSO4•5H2O,是纯净物,故C正确;
D.氯水是氯气的水溶液是混合物,故D错误;
故选C.
点评 本题考查了纯净物和混合物的区别,抓住物质是由几种物质组成的,如果只有一种物质组成就属于纯净物,如果有多种物质就属于混合物是解答本题的关键,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
3.“司乐平”是治疗高血压的一种临床药物,其有效成分M的结构简式如图.下列关于M的说法正确的是( )
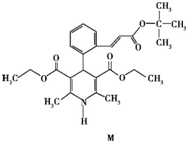

| A. | 属于芳香烃 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 1 mol M完全水解生成2 mol醇 |
4.尿黑酸症是由酪氨酸在人体内非正常代谢而产生的一种疾病.其转化过程如下:
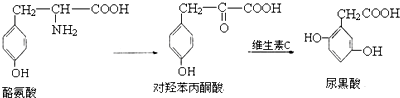
下列说法错误的是( )

下列说法错误的是( )
| A. | 1mol酪氨酸能与含1molHCl的盐酸反应,又能与含2molNaOH的溶液反应 | |
| B. | 酪氨酸能发生加成、取代、消去和缩聚反应 | |
| C. | 1mol对羟苯丙酮酸最多可与5molH2反应 | |
| D. | 1mol尿黑酸最多可与3molBr2反应 |
1.下列实验中,现象和对应结论均正确的是( )
| 选项 | 实 验 | 现 象 | 结 论 |
| A | T℃时,向NaCl和NaBr的混合溶液中滴加AgNO3溶液 | 先出现白色沉淀 | T℃时,Ksp: AgCl<AgBr |
| B | 向等浓度的Na2CO3溶液或Na2SO4溶液中滴加酚酞试剂 | Na2CO3溶液变红色Na2SO4溶液无明显现象 | 非金属性:S>C |
| C | 常温下,取饱和CaSO4溶液或氨水做导电性实验 | 氨水实验的灯泡较亮 | CaSO4和NH3•H2O均为弱电解质 |
| D | 向品红溶液中滴加NaClO溶液或通入SO2气体 | 品红溶液均褪为无色 | 两者均有漂白性且 原理相同 |
| A. | A | B. | B | C. | C | D. | D |
8.化学与社会、科学、技术、环保密切相关.下列有关说法不正确的是( )
| A. | 荧光蛋白是一种高分子化合物且能发生水解 | |
| B. | 用纯碱溶液和盐酸可以清洗锅炉中的硫酸钙 | |
| C. | 利用次氯酸钠溶液的碱性对餐具和环境消毒 | |
| D. | 大量排放PM2.5、SO2、NOX等会形成雾霾 |
18.通过溶解、过滤、蒸发等操作,可以将下列各组固体混合物分离的是( )
| A. | 硝酸钠 氢氧化钠 | B. | 氧化铜 二氧化锰 | ||
| C. | 氯化钾 碳酸钙 | D. | 硫酸铜 氢氧化钠 |
5.(1)由于钠很容易与空气中的二氧化碳和水等物质反应,所以钠在自然界里只能以化合态存在.
(2)维生素C又称为抗坏血酸,在人体内有重要的功能.例如帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+.这说明维生素C具有还原性(填氧化性或还原性).
(3)写出下列空格内物质的名称、俗名或化学式:
(4)写出下列电离方程式或化学方程式:①Na2CO3在水溶液中的电离方程式Na2CO3=2Na++CO32-②曾青(CuSO4)得铁化为铜的化学方程式Fe+CuSO4=Cu+FeSO4.
(2)维生素C又称为抗坏血酸,在人体内有重要的功能.例如帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+.这说明维生素C具有还原性(填氧化性或还原性).
(3)写出下列空格内物质的名称、俗名或化学式:
| 名称 | 氧化铁 | 碳酸钠 | 碳酸氢钠 |
| 俗名 | 铁红 | 小苏打 | |
| 化学式 | Na2CO3 | NaHCO3 |
3.明代宋应星在《天工开物》对“膏夜”的描述:“草木之实,其中蕴藏膏液而不能自流.假媒水火,凭借木石,而后倾注而出焉.”、“榨出水油清亮无比,贮小盏之中,独根心草燃至天明,盖诸清油所不及者.”,下列有关说法中正确的是( )
| A. | “膏液”的主要成分是石油 | B. | “膏液”是天然高分子化合物 | ||
| C. | “膏液”是烃的混合物 | D. | “膏液”能发生取代反应 |
 ,很多不饱和有机物在E催化下可与H2加成反应:
,很多不饱和有机物在E催化下可与H2加成反应: