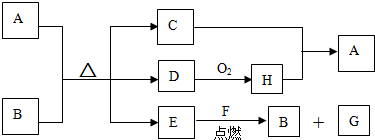
20.下列物质不能使酸性高锰酸钾溶液褪色的是( )
| A. | 甲苯 | B. | 苯 | C. | 乙烯 | D. | 乙炔 |
18.下列关于有机物的说法中,正确的是( )
| A. | 乙醇和乙酸分子中均含有一OH,均可与NaOH反应 | |
| B. | 甲烷和乙烯均能使酸性的高锰酸钾溶液褪色 | |
| C. | 苯分子是一种单双键交替排列的特殊结构,所以既可发生取代又能加成反应 | |
| D. | 煤和石油均为混合物 |
17.下列各组物质互为同分异构体的是( )
| A. | 乙烷和乙烯 | B. | 乙醇与乙醛 | ||
| C. | 乙酸与甲酸甲酯(HCOOCH3) | D. | 淀粉和纤维素 |
16.下列叙述正确的是( )
| A. | 原子半径:Al>Mg>Na>H | B. | 热稳定性:NH3>PH3>H2S>HCl | ||
| C. | 酸性:HClO4>H2SiO3>H3PO4>H2CO3 | D. | 元素非金属性:F>O>N>C |
15.下列实验方法不合理的是( )
| A. | 利用NaOH溶液可以鉴别Al2(SO4)3、MgCl2和Fe2(SO4)3三种溶液 | |
| B. | 用焰色反应可以鉴别出NaCl和K2SO4两种无色溶液 | |
| C. | 用氢氧化钠溶液可以鉴别NH4Cl和NH4NO3两种物质 | |
| D. | 用丁达尔效应可以鉴别氢氧化铝胶体和氯化铝溶液 |
14.以下物质间的每步转化通过一步反应不能实现的是( )
| A. | S→SO3→H2SO4→SO2 | B. | N2→NO→NO2→HNO3 | ||
| C. | Na→Na2O→NaOH→Na2CO3 | D. | Al→Al2O3→Al2(SO4)3→Al(OH)3 |
13.下列四个反应中,水起的作用与其它反应不同的是( )
| A. | NO2+H2O | B. | Cl2+H2O | C. | Na+H2O | D. | SO2+H2O |
12.下列操作中,溶液的颜色不发生变化的是( )
| A. | 碳酸氢钠溶液中滴加稀盐酸 | B. | 硫酸铁溶液中滴加硫氰化钾溶液 | ||
| C. | 碘水中滴加淀粉碘化钾溶液 | D. | 氯化铁溶液中加入还原性铁粉 |
11.如图所示装置是“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中是否有CO2和CO.(图中夹持装置及尾气处理装置均已略去)
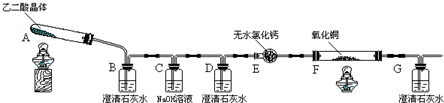
(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳.
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊.
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊.
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量红色固体,滴加稀硫酸,观察红色固体是否有部分溶解,溶液是否变蓝色.
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4氧化生成CO2.KMnO4和草酸钠在稀硫酸中反应的离子方程式是:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
KMnO4溶液的物质的量浓度的计算式是c(KMnO4)=$\frac{0.2000g×2mol}{5mol×134g/mol×0.01601L}$.
0 154540 154548 154554 154558 154564 154566 154570 154576 154578 154584 154590 154594 154596 154600 154606 154608 154614 154618 154620 154624 154626 154630 154632 154634 154635 154636 154638 154639 154640 154642 154644 154648 154650 154654 154656 154660 154666 154668 154674 154678 154680 154684 154690 154696 154698 154704 154708 154710 154716 154720 154726 154734 203614

(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳.
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊.
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊.
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量红色固体,滴加稀硫酸,观察红色固体是否有部分溶解,溶液是否变蓝色.
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4氧化生成CO2.KMnO4和草酸钠在稀硫酸中反应的离子方程式是:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |