20. S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
①CS2+3Cl2$\stackrel{50-60℃}{→}$CCl4+S2Cl2;
②2S+Cl2$\stackrel{90-100℃}{→}$S2Cl2.
已知S2Cl2中硫元素显+1价,S2Cl2不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).
反应涉及的几种物质的熔沸点如表:
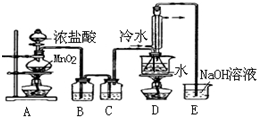
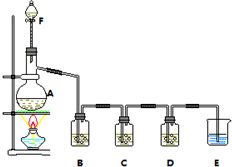
实验室利用下列装置通过方法①来制备S2Cl2(部分夹持仪器已略去).回答下列问题:
(1)S2Cl2分子中各原子都满足最外层8电子结构,则其电子式为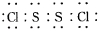 .
.
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(4)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中BC实验.
A.银镜反应 B.制取乙酸乙酯 C.制取溴苯 D.制备乙烯
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是防止倒吸.
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清且生成两种有刺激性气味的气体,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的浓氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是ClO-+2H++Cl-=Cl2↑+H2O.(用离子方程式表示)
 S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:①CS2+3Cl2$\stackrel{50-60℃}{→}$CCl4+S2Cl2;
②2S+Cl2$\stackrel{90-100℃}{→}$S2Cl2.
已知S2Cl2中硫元素显+1价,S2Cl2不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).
反应涉及的几种物质的熔沸点如表:
实验室利用下列装置通过方法①来制备S2Cl2(部分夹持仪器已略去).回答下列问题:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
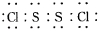 .
.(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(4)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中BC实验.
A.银镜反应 B.制取乙酸乙酯 C.制取溴苯 D.制备乙烯
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是防止倒吸.
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清且生成两种有刺激性气味的气体,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的浓氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是ClO-+2H++Cl-=Cl2↑+H2O.(用离子方程式表示)
16.关于苯的下列说法正确的是( )
0 154466 154474 154480 154484 154490 154492 154496 154502 154504 154510 154516 154520 154522 154526 154532 154534 154540 154544 154546 154550 154552 154556 154558 154560 154561 154562 154564 154565 154566 154568 154570 154574 154576 154580 154582 154586 154592 154594 154600 154604 154606 154610 154616 154622 154624 154630 154634 154636 154642 154646 154652 154660 203614
| A. | 苯是1825年由俄国科学家门捷列夫发现的 | |
| B. | 苯与乙烯一样,是很重要的化工原料,可作消毒剂、有机溶剂、洗涤剂 | |
| C. | 苯的分子式中碳原子远没有饱和,因此能使溴水和高锰酸钾褪色 | |
| D. | 苯环上的碳碳键是一种介于单键和双键的独特的键,苯既能发生取代反应也能发生加成反应 |
 .
.
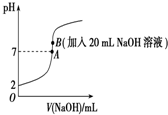 25℃下,向20mL 0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示,请回答下列问题:
25℃下,向20mL 0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示,请回答下列问题: 近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体.为减少“雾霾”的发生,可采取以下措施:
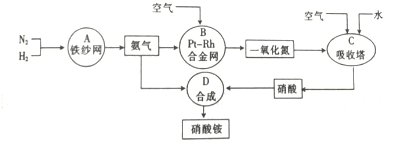
近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体.为减少“雾霾”的发生,可采取以下措施: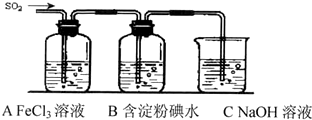
 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.