4.无机化学命名委员会在1989年作出决定:把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列.按这个规定,下列说法正确的是( )
| A. | 第3列元素种类最多 | |
| B. | 每一列都有非金属元素 | |
| C. | 从上到下第1列元素的单质熔点逐渐升高,而第17列元素的单质熔点逐渐降低 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
2.已知反应2A(g)?2B(g)+C(s),某温度下的平衡常数为4,此温度下,在2L的密闭容器中加入amolA,反应到某时刻测得各组分的浓度如表,则下列说法中正确的是( )
| 物质 | A | B |
| 浓度/(mol•L-1) | 0.4 | 0.6 |
| A. | a=1.0 | |
| B. | 此时刻正反应速率小于逆反应速率 | |
| C. | 在相同条件下,若起始时加入2amolA,则达到平衡时A的转化率减小 | |
| D. | 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 |
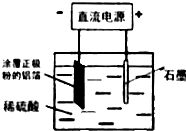
20.甲,乙两同学用图所示装置进行实验探究硝酸与铁反应的产物.

文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO?Fe(NO)SO4(棕色)△H<0.
Ⅲ.NO2和NO都能被KMnO4氧化吸收
Ⅳ.铁氰化钾化学式为K3[Fe(CN)6]:亚铁氰化钾化学式为K4[Fe(CN)6]
3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓(蓝色沉淀)
甲的实验操作和现象记录如下:
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)甲的实验操作中通入CO2的目的是排除反应体系中的空气,防止对产物中有无一氧化氮判断的干扰.
(3)甲取少量B中溶液,加热,棕色溶液变浅绿色,有无色气体逸出,且在空气中变为红棕色其原因是FeSO4+NO?Fe(NO)SO4(棕色)△H<0,正反应放热,加热后,平衡向逆反应方向移动,甲依据该现象得出的结论是A中有NO生成.
(4)乙认为甲得出A中有NO生成的证据不足.为获取充足的证据,乙仍采用该装置和操作进行对照实验,浓硝酸换成稀硝酸浓硝酸换成稀硝酸,证明有NO生成的实验现象是A中没有红棕色气体生成,B中溶液变为棕色.
(5)将A所得溶液稀释至500mL,取少量稀释后的溶液调节pH后,滴加铁氰化钾溶液有蓝色沉淀生成,由此证明A溶液中含有Fe2+(填离子符号).
另取稀释后的溶液25.00mL加入过量的KI固体,充分反应后pH至7左右,滴入几滴淀粉溶液做指示剂,用0.25mo1/L Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3溶液16.00mL.(己知:I2+2S2O32-=2I-+S4O62-),则A中所得溶液的c(Fe3+)=0.16mo1/L.

文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO?Fe(NO)SO4(棕色)△H<0.
Ⅲ.NO2和NO都能被KMnO4氧化吸收
Ⅳ.铁氰化钾化学式为K3[Fe(CN)6]:亚铁氰化钾化学式为K4[Fe(CN)6]
3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓(蓝色沉淀)
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余,得100mL的溶液 |
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)甲的实验操作中通入CO2的目的是排除反应体系中的空气,防止对产物中有无一氧化氮判断的干扰.
(3)甲取少量B中溶液,加热,棕色溶液变浅绿色,有无色气体逸出,且在空气中变为红棕色其原因是FeSO4+NO?Fe(NO)SO4(棕色)△H<0,正反应放热,加热后,平衡向逆反应方向移动,甲依据该现象得出的结论是A中有NO生成.
(4)乙认为甲得出A中有NO生成的证据不足.为获取充足的证据,乙仍采用该装置和操作进行对照实验,浓硝酸换成稀硝酸浓硝酸换成稀硝酸,证明有NO生成的实验现象是A中没有红棕色气体生成,B中溶液变为棕色.
(5)将A所得溶液稀释至500mL,取少量稀释后的溶液调节pH后,滴加铁氰化钾溶液有蓝色沉淀生成,由此证明A溶液中含有Fe2+(填离子符号).
另取稀释后的溶液25.00mL加入过量的KI固体,充分反应后pH至7左右,滴入几滴淀粉溶液做指示剂,用0.25mo1/L Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3溶液16.00mL.(己知:I2+2S2O32-=2I-+S4O62-),则A中所得溶液的c(Fe3+)=0.16mo1/L.
16.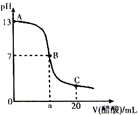 在20mL0.100mol•L-1NaOH溶液中逐滴加入0.200mol•L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较正确的是( )
在20mL0.100mol•L-1NaOH溶液中逐滴加入0.200mol•L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较正确的是( )
0 154455 154463 154469 154473 154479 154481 154485 154491 154493 154499 154505 154509 154511 154515 154521 154523 154529 154533 154535 154539 154541 154545 154547 154549 154550 154551 154553 154554 154555 154557 154559 154563 154565 154569 154571 154575 154581 154583 154589 154593 154595 154599 154605 154611 154613 154619 154623 154625 154631 154635 154641 154649 203614
 在20mL0.100mol•L-1NaOH溶液中逐滴加入0.200mol•L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较正确的是( )
在20mL0.100mol•L-1NaOH溶液中逐滴加入0.200mol•L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较正确的是( )| A. | A点到B点的变化过程中,离子浓度大小关系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 在B点a>10,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) | |
| C. | B点到C点的变化过程中,离子浓度大小关系:c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| D. | 在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
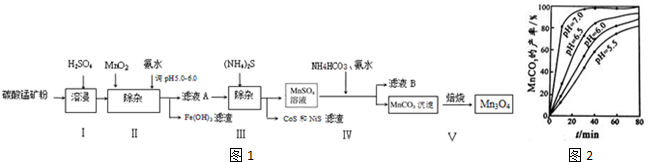

 氯化铜、氯化亚铜是重要的化工原料,广泛用作有机合成催化剂.
氯化铜、氯化亚铜是重要的化工原料,广泛用作有机合成催化剂. a、b、c、d是四种原子序数依次增大的短周期元素.a原子的电子层数为n,核内质子数是2n2-1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的.回答下列问题:
a、b、c、d是四种原子序数依次增大的短周期元素.a原子的电子层数为n,核内质子数是2n2-1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的.回答下列问题: