6.vL Fe2(SO4)3溶液中含有a克SO42-,取此溶液0.5vL,用水稀释至2vL,则稀释后溶液中Fe3+的物质的量的浓度为( )
| A. | $\frac{a}{576v}$mol/L | B. | $\frac{125a}{36v}$mol/L | C. | $\frac{250a}{36v}$mol/L | D. | $\frac{250a}{48v}$mol/L |
5.下列叙述错误的是( )
| A. | 标准状况下,5L CH4气体与5L NH3气体的原子个数之比为5:4 | |
| B. | 常温常压下,11.2L O3中所含氧原子个数大于1.5NA | |
| C. | 同温、同压下,相同体积的N2和CO气体具有相同的分子数和相同的密度 | |
| D. | 同温、同压下,等质量的一氧化碳和二氧化碳的密度比为11:7 |
4.下列物质之间的相互关系不正确的是( )
| A. | CH3-CH2-NO2和H2N-CH2-COOH互为同分异构体 | |
| B. | O2和O3互为同素异形体 | |
| C. | H、D、T互为同位素 | |
| D. | 干冰和冰为同一种物质 |
3.常温下向25mL 0.1mol.L-1NaOH溶液中逐滴滴加0.2mol•L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )


| A. | 水电离出的c(H+):A点小于B点 | |
| B. | 在B点,离子浓度大小为c(OH-)>c(H+)>c(Na+)>c(N3-) | |
| C. | 在C点,滴加的V(HN3)=12.5 mL | |
| D. | 在D点,c(Na+)=2c(HN3)+2 c(N3-) |
1.在100mLNa2CO3与NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系,如图所示.下列说法正确的是( )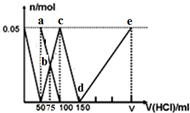

| A. | a点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-) | |
| B. | b点所得溶液中阴离子浓度大小顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | c点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO32-)=1.5 mol•L-1 | |
| D. | d→e的过程中水的电离程度逐渐减小 |
20.下列说法正确的是( )
| A. | 不同元素的原子发生跃迁时,会释放不同的光 | |
| B. | 第一电离能与电负性的数值都是以气态中性基态原子为研究对象测得到 | |
| C. | 分子中的原子有固定的空间位置,组成完全相同的分子,由于原子位置的不同会表现出不同的性质 | |
| D. | 两个相同的原子的任意未成对电子的电子云在两个原子核间重叠,形成非极性共价键 |
19.下列物质与苯互为同系物的是( )
| A. |  | B. |  | C. |  | D. |  |
18. 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷
( ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
以下是实验步骤:
步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L一1浓盐酸,充分溶解、冷却,再加入2一丁
醇,加热一段时间.
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分.
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水
洗涤,再加入CaCl2固体,放置一段时间后过滤.
步骤4:滤液经进一步精制得产品
(1)加入烧瓶的物质中,有一种是催化剂,该物质是无水ZnCl2.
(2)反应装置中冷凝管的作用是冷凝回流提高原料利用率,烧杯内所盛液体可以是水或碱液.
(3)用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,第二次用蒸馏水
洗涤的目的是除去残留的氢氧化钠.
(4)步骤4精制过程中不需使用的仪器是ad.
a.布氏漏斗b.抽滤瓶c.蒸馏烧瓶d.冷凝管.
 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷(
 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L一1浓盐酸,充分溶解、冷却,再加入2一丁
醇,加热一段时间.
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分.
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水
洗涤,再加入CaCl2固体,放置一段时间后过滤.
步骤4:滤液经进一步精制得产品
(1)加入烧瓶的物质中,有一种是催化剂,该物质是无水ZnCl2.
(2)反应装置中冷凝管的作用是冷凝回流提高原料利用率,烧杯内所盛液体可以是水或碱液.
(3)用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,第二次用蒸馏水
洗涤的目的是除去残留的氢氧化钠.
(4)步骤4精制过程中不需使用的仪器是ad.
a.布氏漏斗b.抽滤瓶c.蒸馏烧瓶d.冷凝管.
17.部分弱电解质的电离平衡常数如下表,下列说法不正确的是( )
0 154365 154373 154379 154383 154389 154391 154395 154401 154403 154409 154415 154419 154421 154425 154431 154433 154439 154443 154445 154449 154451 154455 154457 154459 154460 154461 154463 154464 154465 154467 154469 154473 154475 154479 154481 154485 154491 154493 154499 154503 154505 154509 154515 154521 154523 154529 154533 154535 154541 154545 154551 154559 203614
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3•H2O |
| 电离平衡常数 (25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
| A. | 25℃时,若将pH=3的盐酸与pH=11的氨水混合后溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水) | |
| B. | 0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 结合H+的能力:CO32->HCO3->CN->HCOO- | |
| D. | 0.1mol/L的NaHCO3溶液中:c(H2CO3)+c(H+)=c(OH-)+c(CO32-) |

