4.如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
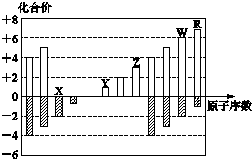

| A. | 离子半径:Z>Y>X | |
| B. | 最高正价氧化物对应的水化物的酸性:R<W | |
| C. | 氢化物的还原性:R>W | |
| D. | R的单质能与W的氢化物反应,可证明非金属性:R>W |
3.下列说法错误的是( )
| A. | 金属在原电池中做正极被保护 | |
| B. | 原电池中阴离子向负极移动 | |
| C. | 常温下,强酸强碱在稀溶液中反应的中和热是-57.3KJ.mol-1 | |
| D. | 用惰性电极电解CuSO4溶液,外电路中每通过1mol电子,溶液中就产生1mol H+ |
1.I.现有下列8种物质
①NaHCO3②NH4HCO3③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH
其中属于强电解质的是①②③(填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是①②⑥.
II.现有一瓶浓度为0.2mol/L的某酸溶液,可能为醋酸、盐酸、硫酸中的一种,为了确定该酸溶液的组成进行实验:取20.00mL该酸溶液,逐滴加入0.2mol/L的氢氧化钠溶液,恰好反应完全时所需碱液体积为20.00mL,请用化学用语回答:
(1)该酸不可能是H2SO4;
(2)用pH试纸测得反应后所得溶液呈碱性,根据此现象说明该酸溶液为醋酸,用离子方程式说明溶液呈碱性的原因CH3COO-+H2O?CH3COOH+OH-
III.A、B、C、D均为可溶于水的固体,组成它们的离子有:
分别取它们的水溶液进行实验,结果如下:
①A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会消失.
②C与D反应有红褐色沉淀生成并放出气体.
③B与C反应有白色沉淀生成并放出气体.
(1)写出它们的化学式:ABa(OH)2,BAl2(SO4)3,CK2CO3,DFe(NO3)3.
(2)写出③中B与C反应的离子方程式2Al3++3CO32-+3H2O=2Al(OH)3↓+CO2↑.
①NaHCO3②NH4HCO3③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH
其中属于强电解质的是①②③(填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是①②⑥.
II.现有一瓶浓度为0.2mol/L的某酸溶液,可能为醋酸、盐酸、硫酸中的一种,为了确定该酸溶液的组成进行实验:取20.00mL该酸溶液,逐滴加入0.2mol/L的氢氧化钠溶液,恰好反应完全时所需碱液体积为20.00mL,请用化学用语回答:
(1)该酸不可能是H2SO4;
(2)用pH试纸测得反应后所得溶液呈碱性,根据此现象说明该酸溶液为醋酸,用离子方程式说明溶液呈碱性的原因CH3COO-+H2O?CH3COOH+OH-
III.A、B、C、D均为可溶于水的固体,组成它们的离子有:
| 阳离子 | K+、Ba2+、Al3+、Fe3+ |
| 阴离子 | OH-、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ |
①A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会消失.
②C与D反应有红褐色沉淀生成并放出气体.
③B与C反应有白色沉淀生成并放出气体.
(1)写出它们的化学式:ABa(OH)2,BAl2(SO4)3,CK2CO3,DFe(NO3)3.
(2)写出③中B与C反应的离子方程式2Al3++3CO32-+3H2O=2Al(OH)3↓+CO2↑.
20.下列物质能使KMnO4酸性溶液褪色,不能使溴水褪色的是( )
| A. | 苯 | B. | 丙烯 | C. | 二甲苯 | D. | 己烷 |
15.某化学研究性学习小组拟测定食醋的总酸量(g/10mL),请你参与该小组的实验并回答相关问题.
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500mL(商标注明总酸量:3,.50g/100mL~5.00g/100mL),0.1000mol/L NaOH标准溶液;100mL容量瓶,10mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙,酚酞,石蕊).
[实验步骤]
①配制并移取待测食醋溶液
用10mL移液管吸取10mL市售白醋样品置于100mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20mL,并移至锥形瓶中.
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下.静置,读取数据并记录为NaOH标准溶液体积的初读数.
③滴定
往盛有待测食醋溶液的锥形瓶中的滴加某酸碱指示计2~3滴,滴定至终点.记录NaOH的终读数.重复滴定3次.
[数据记录]
[问题与思考]
(1)步骤①中用煮沸并迅速冷却的方法处理蒸馏水的目的是除去CO2,防止其对实验结果的影响.
(2)步骤③中你选择的酸碱指示剂是酚酞,理由是CH3COONa溶液呈碱性,应选择变色范围在碱性的指示剂.
(3)样品总酸量=4.50g/100mL.
(4)导致实验结果偏大的主要原因是①②(填写序号)
①滴定终点时,仰视滴定管读数
②滴定后滴定管尖嘴处悬有一滴液体
③移液管用蒸馏水洗净后,就用来吸取待测液
④滴定前,碱式滴定管无气泡,滴定后产生气泡
⑤锥形瓶只用蒸馏水洗涤后仍留有少量蒸馏水.
0 154313 154321 154327 154331 154337 154339 154343 154349 154351 154357 154363 154367 154369 154373 154379 154381 154387 154391 154393 154397 154399 154403 154405 154407 154408 154409 154411 154412 154413 154415 154417 154421 154423 154427 154429 154433 154439 154441 154447 154451 154453 154457 154463 154469 154471 154477 154481 154483 154489 154493 154499 154507 203614
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500mL(商标注明总酸量:3,.50g/100mL~5.00g/100mL),0.1000mol/L NaOH标准溶液;100mL容量瓶,10mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙,酚酞,石蕊).
[实验步骤]
①配制并移取待测食醋溶液
用10mL移液管吸取10mL市售白醋样品置于100mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20mL,并移至锥形瓶中.
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下.静置,读取数据并记录为NaOH标准溶液体积的初读数.
③滴定
往盛有待测食醋溶液的锥形瓶中的滴加某酸碱指示计2~3滴,滴定至终点.记录NaOH的终读数.重复滴定3次.
[数据记录]
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(样品)/ml | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)始/ml | 0.00 | 0.20 | 0.10 | 0.10 |
| V(NaOH)终/ml | 14.98 | 15.20 | 15.12 | 16.24 |
(1)步骤①中用煮沸并迅速冷却的方法处理蒸馏水的目的是除去CO2,防止其对实验结果的影响.
(2)步骤③中你选择的酸碱指示剂是酚酞,理由是CH3COONa溶液呈碱性,应选择变色范围在碱性的指示剂.
(3)样品总酸量=4.50g/100mL.
(4)导致实验结果偏大的主要原因是①②(填写序号)
①滴定终点时,仰视滴定管读数
②滴定后滴定管尖嘴处悬有一滴液体
③移液管用蒸馏水洗净后,就用来吸取待测液
④滴定前,碱式滴定管无气泡,滴定后产生气泡
⑤锥形瓶只用蒸馏水洗涤后仍留有少量蒸馏水.
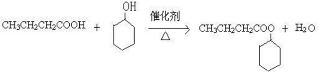 .
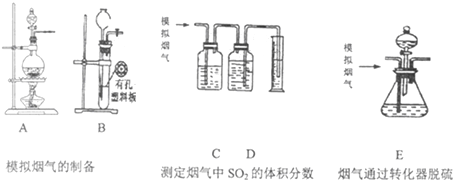
.
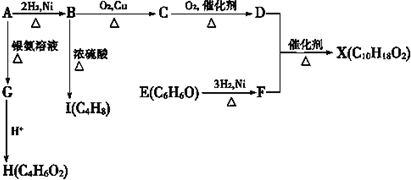
 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:


 .
. .
. .
. .
. 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.