题目内容
17.肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:①N2(g)+2O2(g)═N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)═N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应的热化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
(2)上述反应中氧化剂是N2O4.
(3)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)?2NO2(g)
①上述反应的△H>0(选填“>”或“<”).
②保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,再次达到平衡时,混合气体中NO2的体积分数减小(填“增大”、“减小”或“不变”),混合气体的颜色变深(填“变深”或“变浅”).
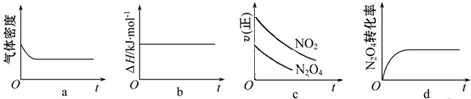
③一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是ad.
④若在相同温度下,上述反应改在体积为10L的恒容密闭容器中进行,反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=0.01 mol•L-1•s-1.
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为N2H4+4OH--4e-=4H2O+N2↑.
分析 (1)已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5 kJ•mol-1,②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2 kJ•mol-1,则根据盖斯定律可知②×2-①即可得到热化学方程式;
(2)反应中,N2O4(l)中N元素化合价从+4价就得到0价,得电子发生还原反应是氧化剂;
(3)①升高温度,化学平衡向吸热反应方向移动,当温度升高时,气体颜色变深,平衡向正反应方向移动,升温平衡向吸热反应方向进行;
②保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,相对于成比例增大反应物,即增大压强平衡向气体体积减小的方向移动即逆反应方向,所以NO2的体积分数减小,但二氧化氮的浓度仍然增大,则混合气体的颜色变深;
③a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态;
b、反应过程中,反应热不会变化;
c、根据图象,正反应速率仍然是变化的;
d、四氧化二氮的转化率不变,说明正逆反应速率相等;
④化学平衡常数只与温度有关,与物质的浓度无关,所以平衡常数K不变;v(NO2))=$\frac{△c}{△t}$;
(4)原电池中负极失去电子,发生氧化反应,则肼在负极通入,又因为溶液显碱性,则负极反应式为N2H4+4OH--4e-=4H2O+N2↑.
解答 解:(1)已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5 kJ•mol-1,②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2 kJ•mol-1,则根据盖斯定律可知②×2-①即可得到2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9 kJ/mol,
故答案为;2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
(2)反应中,N2O4(l)中N元素化合价从+4价就得到0价,得电子发生还原反应,N2O4(l)是氧化剂,
故答案为:N2O4;
(3)①升高温度,化学平衡向吸热反应方向移动,当温度升高时,气体颜色变深,平衡向正反应方向移动,所以正反应是吸热反应即△H>0,
故答案为:>;
②保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,相对于成比例增大反应物,即增大压强平衡向气体体积减小的方向移动即逆反应方向,所以NO2的体积分数减小,但二氧化氮的浓度仍然增大,则混合气体的颜色变深,
故答案为:减小,变深;
③a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态,故a正确;
b、反应过程中,反应热不会变化,不是变量,无法判断是否达到平衡状态,故b错误;
c、根据图象,正反应速率仍然是变化的,则不能说明达到了平衡状态,故c错误;
d、四氧化二氮的转化率不变,说明正逆反应速率相等,达到了平衡状态,故d正确,
故答案为:ad;
④化学平衡常数只与温度有关,与物质的浓度无关,所以平衡常数K不变;v(NO2))=$\frac{△c}{△t}$═0.02mol/(L•s),则v(N2O4)=$\frac{1}{2}$v(NO2)=0.01mol/(L•s),
故答案为:0.01;
(4)原电池中负极失去电子,发生氧化反应,则肼在负极通入,又因为溶液显碱性,则负极反应式为N2H4+4OH--4e-=4H2O+N2↑.
故答案为:N2H4+4OH--4e-=4H2O+N2↑;
点评 本题考查盖斯定律、化学反应速率和化学平衡影响因素分析、电极反应式的书写等知识点,这些都是高考的热点,注意电极反应式的书写要结合电解质溶液的酸碱性,影响化学平衡的因素分析判断,题目难度中等.

 快捷英语周周练系列答案
快捷英语周周练系列答案| 选项 | 离子组 | 分析 |
| A | Na+、Cu2+、SO42-、Cl- | 能大量共存于同一溶液中,通入过量NH3最终产生蓝色沉淀 |
| B | NH4+、Al3+、S2-、Cl- | 不能大量共存于同一溶液中,因为有Al2S3沉淀产生 |
| C | H+、Fe2+、SO42-、Cl- | 能大量共存于同一溶液中,加入KNO3固体后溶液颜色发生变化 |
| D | Na+、K+、HCO3-、OH- | 不能大量共存于同一溶液中,因为HCO3-与OH-反应有CO2生成 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 钠与氧气 | B. | 氢氧化钠和二氧化碳 | ||
| C. | 氢氧化钠和氯化铝 | D. | 氧化钠和二氧化碳 |
| A. | 2mol/L的Na2CO3溶液中Na+个数为4NA | |
| B. | 2L 0.5mol/LCH3COOH溶液中含有的H+数为NA | |
| C. | 含2mol溶质的浓硫酸与足量的Cu反应转移的电子数为2NA | |
| D. | 1L 2mol/L的K2CO3溶液中CO32-个数小于2NA |
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ | |
| D. | 加热溶液,产生的气体能使湿润的蓝色石蕊试纸变红,一定是NH3 |