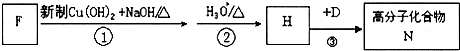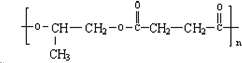8.化学键的键能是指气态原子间形成1mol化学键时释放的能量.如H-I键的键能为297KJ•mol-1,也可以理解为破坏1mol H-I键需要吸收297KJ的热量.一个化学反应一般都有旧化学键的破坏和新化学键的形成.
下表是一些键能数据(KJ•mol-1):
回答下列问题:
由表中数据能否得出这样的结论:
(1)半径越小的原子形成的共价键越牢固(即键能越大)不能(填“能”或“不能”)
(2)非金属性越强的原子形成的共价键越牢固不能(填“能”或“不能”).能否从数据找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;
(3)试预测C-Br键的键能范围218KJ•mol-1<C-Br键能<330KJ•mol-1.
下表是一些键能数据(KJ•mol-1):
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | C-F | 427 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
由表中数据能否得出这样的结论:
(1)半径越小的原子形成的共价键越牢固(即键能越大)不能(填“能”或“不能”)
(2)非金属性越强的原子形成的共价键越牢固不能(填“能”或“不能”).能否从数据找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;
(3)试预测C-Br键的键能范围218KJ•mol-1<C-Br键能<330KJ•mol-1.
4.煤与水在高温下的气化是高效、清洁地利用煤炭的重要途径,其处理方法是将煤转化为( )
| A. | 水煤气 | B. | 干馏煤气 | C. | 天然气 | D. | 焦炭 |
3.下列有关元素或化合物性质的比较不正确的是( )
| A. | 酸性:H2SO4>H2SO3 | B. | 氧化性:H2SO4(浓)>H2SO4(稀) | ||
| C. | 稳定性:CH4<SiH4 | D. | 碱性:Mg(OH)2>Al(OH)3 |
1.下列分子中,所有原子都处于同一平面上的是( )
| A. | 丁烯 | B. | 丙炔 | C. | 乙烷 | D. | 苯 |
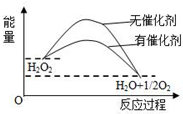
20.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示.下列说法正确的是( )
0 154269 154277 154283 154287 154293 154295 154299 154305 154307 154313 154319 154323 154325 154329 154335 154337 154343 154347 154349 154353 154355 154359 154361 154363 154364 154365 154367 154368 154369 154371 154373 154377 154379 154383 154385 154389 154395 154397 154403 154407 154409 154413 154419 154425 154427 154433 154437 154439 154445 154449 154455 154463 203614

| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+$\frac{1}{2}$O2+Q | |
| D. | 反应物的总能量高于生成物的总能量 |
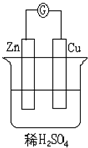 如图,请读题并填空:在图中,
如图,请读题并填空:在图中,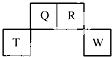 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,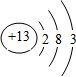 .
.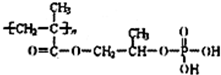
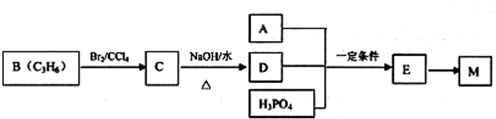
 ,该反应类型是酯化反应.
,该反应类型是酯化反应.