16.通过下列有关操作可以实现以一氯乙烷为原料制取乙二酸(HOOC-COOH),最合理的操作顺序是( )
①与NaOH的水溶液共热 ②与NaOH的醇溶液共热 ③与浓硫酸共热到170℃
④一定条件下与氯气加成 ⑤在Cu或Ag存在的情况下与氧气共热 ⑥与新制的Cu(OH)2共热.
①与NaOH的水溶液共热 ②与NaOH的醇溶液共热 ③与浓硫酸共热到170℃
④一定条件下与氯气加成 ⑤在Cu或Ag存在的情况下与氧气共热 ⑥与新制的Cu(OH)2共热.
| A. | ②④①⑤⑥ | B. | ②④①⑥⑤ | C. | ①③④②⑤ | D. | ①③④②⑥ |
15.有关如图所示化合物的说法不正确的是( )
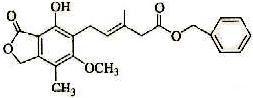

| A. | 一定条件下,既可以与Br2发生加成反应,又可以与Br2发生取代反应 | |
| B. | 1 mol该化合物最多可以与3 molNaOH反应 | |
| C. | 既可以催化加氢,又可以在稀硫酸存在下水解得2种有机物 | |
| D. | 可以与Na2CO3溶液反应放出CO2气体 |
14.有机物CH2=CHCH2CH(OH)COOH在不同条件下至少可能发生7种不同类型的反应:①取代 ②加成 ③消去 ④氧化 ⑤酯化 ⑥缩聚 ⑦加聚,其中可能由于分子结构中含有“-OH”而发生的反应( )
| A. | ①③⑤⑦ | B. | ②④⑥⑦ | C. | ②③④⑤ | D. | ①③④⑤⑥ |
12.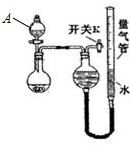 镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
①镁、铝、锌都是银白色的金属
②锌(Zn)可以与NaOH溶液反应生成H2
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3•H2O
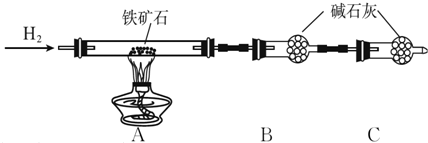
④Zn2+易形成配合物如[Zn(NH3)4]2+,该配合物遇强酸分解生成Zn2+、NH4+(1)(1)甲同学取镁铝合金进行定量分析,用图所示装置进行实验,获得如下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
(2)乙同学取镁铝锌合金设计如下实验方案:
(可用试剂:样品、pH试纸、稀硫酸、NaOH溶液、氨水)
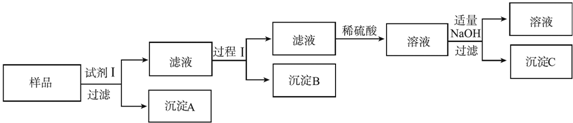
①试剂Ⅰ是NaOH溶液;沉淀B是Al(OH)3.
②过程Ⅰ是:在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入足量的稀氨水,过滤.
③沉淀C与氨水反应的离子方程式为Zn(OH)2+4NH3=[Zn(NH3)4]2++2OH-;或Zn(OH)2+4NH3•H2O=[Zn(NH3)4]2++2OH-+4H2O.
 镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:①镁、铝、锌都是银白色的金属
②锌(Zn)可以与NaOH溶液反应生成H2
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3•H2O
④Zn2+易形成配合物如[Zn(NH3)4]2+,该配合物遇强酸分解生成Zn2+、NH4+(1)(1)甲同学取镁铝合金进行定量分析,用图所示装置进行实验,获得如下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 粉末质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 2.0 g | 10.0 mL | 346.2 mL |
| ② | 2.0 g | 10.0 mL | 335.0 mL |
| ③ | 2.0 g | 10.0 mL | 345.8 mL |
(可用试剂:样品、pH试纸、稀硫酸、NaOH溶液、氨水)

①试剂Ⅰ是NaOH溶液;沉淀B是Al(OH)3.
②过程Ⅰ是:在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入足量的稀氨水,过滤.
③沉淀C与氨水反应的离子方程式为Zn(OH)2+4NH3=[Zn(NH3)4]2++2OH-;或Zn(OH)2+4NH3•H2O=[Zn(NH3)4]2++2OH-+4H2O.
10.在体积为V L的密闭容器中通入a mol NO和b mol O2,反应后容器中氮原子数和氧原子数之比为( )
0 154038 154046 154052 154056 154062 154064 154068 154074 154076 154082 154088 154092 154094 154098 154104 154106 154112 154116 154118 154122 154124 154128 154130 154132 154133 154134 154136 154137 154138 154140 154142 154146 154148 154152 154154 154158 154164 154166 154172 154176 154178 154182 154188 154194 154196 154202 154206 154208 154214 154218 154224 154232 203614
| A. | $\frac{a}{b}$ | B. | $\frac{a}{2b}$ | C. | $\frac{a}{a+2b}$ | D. | $\frac{b}{a}$ |
 .
.