7. 合成氨工业对国民经济和社会发展具有重要的意义,其原理是:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,
合成氨工业对国民经济和社会发展具有重要的意义,其原理是:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,
(1)已知合成氨反应在某温度下2L的密闭容器中进行,测得数据如表:
根据表中数据计算:
①0 min~1 min内N2的平均反应速率为0.05mol/(L•min)
②该条件下反应的平衡常数k=0.15(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N2、H2、NH3各1mol,化学平衡向正向(填“正向”、“逆向”或“不移动”),该反应的平衡常数k不变(填“变大”“减小”或“不变”)
④能表明该反应达到平衡状态的是B(选填序号)
A.N2的转化率等于NH3的产率 B.混合气体的平均相对分子质量不变
C.v(N2)与v(H2)的比值不变 D.混合气体的密度不变
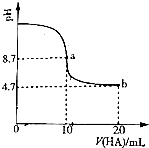
(2)室温下向10mL0.3mol/LNaOH溶液中加入0.3mol/L的一元酸HA溶液pH的变化曲线如图,下列说法正确的是CE.
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A-)>c(HA)
D.pH=7时,c(Na+)=c(A-)+c(HA)
E.b点所示溶液中c(HA)+c(A-)=0.2mol/L.
 合成氨工业对国民经济和社会发展具有重要的意义,其原理是:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,
合成氨工业对国民经济和社会发展具有重要的意义,其原理是:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,(1)已知合成氨反应在某温度下2L的密闭容器中进行,测得数据如表:
| 不同时间各物质的物质的量/mol | |||||
| 0min | 1min | 2min | 3min | 4min | |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
①0 min~1 min内N2的平均反应速率为0.05mol/(L•min)
②该条件下反应的平衡常数k=0.15(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N2、H2、NH3各1mol,化学平衡向正向(填“正向”、“逆向”或“不移动”),该反应的平衡常数k不变(填“变大”“减小”或“不变”)
④能表明该反应达到平衡状态的是B(选填序号)
A.N2的转化率等于NH3的产率 B.混合气体的平均相对分子质量不变
C.v(N2)与v(H2)的比值不变 D.混合气体的密度不变
(2)室温下向10mL0.3mol/LNaOH溶液中加入0.3mol/L的一元酸HA溶液pH的变化曲线如图,下列说法正确的是CE.
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A-)>c(HA)
D.pH=7时,c(Na+)=c(A-)+c(HA)
E.b点所示溶液中c(HA)+c(A-)=0.2mol/L.
3.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 24g Mg变为Mg2+时失去的电子数为2NA | |
| B. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| C. | 常温常压下,22 g氧气和26 g臭氧所含氧原子总数为3 NA | |
| D. | 18 g重水(D2O)所含电子数为10NA |
2.下列关于同分异构体异构方式的说法中,正确的是( )
| A. | CH3CH2CH2CH3和CH3CH(CH3)2属于碳链异构 | |
| B. | 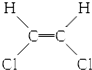 和 和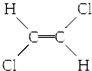 属于位置异构 属于位置异构 | |
| C. | CH2═C(CH3)2和CH3CH═CHCH3属于官能团异构 | |
| D. | CH3CH2CH2COOH和CH3COOCH2CH3属于位置异构 |
1.化学与人们的生活、健康密切相关.下列做法不合理的是( )
| A. | 用米汤检验加碘食盐中的碘酸钾(KIO3) | |
| B. | 向豆浆中加入盐卤(主要成分为MgCl2)制做豆腐 | |
| C. | 用灼烧和闻气味的方法区别棉织物和纯毛织物 | |
| D. | 向污水中加入适量明矾,可除去其中的悬浮物 |
20.下列说法不正确的是( )
| A. | △H<0、△S>0的反应在任何温度下都能自发进行 | |
| B. | NH4HCO3(s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| C. | 硝酸铵固体的溶解过程与焓变有关 | |
| D. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
19.某固体中只可能含Cl-、SO42-、CO32-、Cu2+、Ba2+和Na+.探究小组为了确定该固体的组成,取该固体39g进行以下实验:(填写表中的空格)
(1)步骤二发生反应的离子方程式为2H++CO32-=CO2↑+H2O,步骤四发生反应的离子方程式为Ag++Cl-=AgCl↓.
(2)原固体中含有Na+的理由是溶液呈电中性,必须有阳离子,是否含有Cl-并说明理由碳酸钠与硫酸钠质量之和为39g,则不含氯离子.
0 153969 153977 153983 153987 153993 153995 153999 154005 154007 154013 154019 154023 154025 154029 154035 154037 154043 154047 154049 154053 154055 154059 154061 154063 154064 154065 154067 154068 154069 154071 154073 154077 154079 154083 154085 154089 154095 154097 154103 154107 154109 154113 154119 154125 154127 154133 154137 154139 154145 154149 154155 154163 203614
| 实验操作与现象 | 实验结论 | |
| 步骤一 | 将该固体全部溶于于得无色溶液; | 肯定无Cu2+. |
| 步骤二 | 向上述溶液中加入足量盐酸,产生无色无味的气体共收集到2.24L(标准状况); | 肯定有CO32- 肯定无Ba2+ |
| 步骤三 | 向步骤二所得溶液中继续加入足量BaCl2溶液,产生沉淀,过滤并洗涤干燥后得46.6g白色沉淀. | 肯定有SO42- |
| 步骤四 | 向步骤三所得滤液中加入AgNO3溶液,得白色沉淀. |
(2)原固体中含有Na+的理由是溶液呈电中性,必须有阳离子,是否含有Cl-并说明理由碳酸钠与硫酸钠质量之和为39g,则不含氯离子.