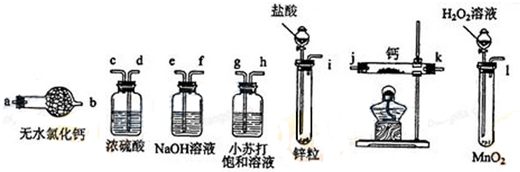
3.某混合溶液中可能大量含有的离子如下表所示:
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示.
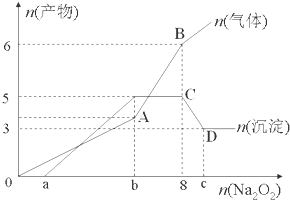
(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)a=1,b=7,c=9.
(3)写出下列离子方程式:
AB段2Na2O2+2H2O=4Na++4OH-+O2↑、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
CD段Al(OH)3+OH-=AlO2-+2H2O.
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |

(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)a=1,b=7,c=9.
(3)写出下列离子方程式:
AB段2Na2O2+2H2O=4Na++4OH-+O2↑、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
CD段Al(OH)3+OH-=AlO2-+2H2O.
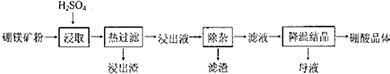
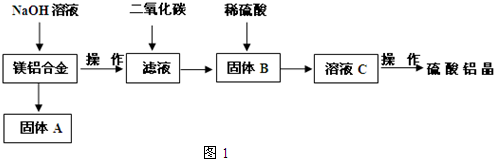
18.用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量红棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2SO4溶解A12O3的化学方程式是Al2O3+3H2SO4=2Al2(SO4)3+3H2O.
(2)KMnO4氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
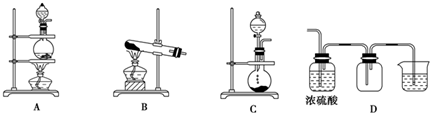
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量红棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2SO4溶解A12O3的化学方程式是Al2O3+3H2SO4=2Al2(SO4)3+3H2O.
(2)KMnO4氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
14.将pH试纸用蒸馏水湿润后,去测定某盐酸的pH,测得的pH将比实际( )
0 153890 153898 153904 153908 153914 153916 153920 153926 153928 153934 153940 153944 153946 153950 153956 153958 153964 153968 153970 153974 153976 153980 153982 153984 153985 153986 153988 153989 153990 153992 153994 153998 154000 154004 154006 154010 154016 154018 154024 154028 154030 154034 154040 154046 154048 154054 154058 154060 154066 154070 154076 154084 203614
| A. | 偏高 | B. | 偏低 | ||
| C. | 不变 | D. | 三种情况均有可能 |
 .
.
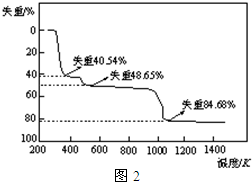 (5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K-523K,553K-687K,1043K以上不再失重,其热分解的TG曲线见图2,已知:失重%=$\frac{加热减少的质量}{原晶体样品的总质量}$×100%.根据图示数据计算确定每步分解的产物,写出第一阶段分解产物的化学式Al2(SO4)3.3H2O,第三阶段反应化学方程式Al2(SO4)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3SO3↑.
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K-523K,553K-687K,1043K以上不再失重,其热分解的TG曲线见图2,已知:失重%=$\frac{加热减少的质量}{原晶体样品的总质量}$×100%.根据图示数据计算确定每步分解的产物,写出第一阶段分解产物的化学式Al2(SO4)3.3H2O,第三阶段反应化学方程式Al2(SO4)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3SO3↑.