题目内容
18.用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O,工艺流程如下(部分操作和条件略):Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量红棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2SO4溶解A12O3的化学方程式是Al2O3+3H2SO4=2Al2(SO4)3+3H2O.
(2)KMnO4氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
分析 (1)氧化铝是两性氧化物溶于强酸强碱;
(2)依据氧化还原反应电子守恒和原子守恒,结合元素化合价变化分析产物和反应物;
(3)依据金属阳离子沉淀开始和完全沉淀需要的溶液PH分析,亚铁离子被氧化为铁离子,调节溶液PH使铁离子全部沉淀;
(4)①浓盐酸和二氧化锰再加热条件下生成黄绿色气体氯气;
②加入MnSO4至紫红色消失,目的是除去过量高锰酸根离子.
解答 解:(1)硫酸溶解氧化铝生成硫酸铝和水,反应的化学方程式为:Al2O3+3H2SO4=2Al2(SO4)3+3H2O;
故答案为:Al2O3+3H2SO4=2Al2(SO4)3+3H2O;
(2)高锰酸根离子在酸溶液中被还原为锰离子,亚铁离子被氧化为铁离子,反应的离子方程式为:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
故答案为:1、5;8H+; 1、5; 4H2O;
(3)向滤液中加入过量KMnO4溶液,目的是氧化亚铁离子为三价铁离子,依据图表数据分析可知,铁离子开始沉淀和沉淀完全的溶液pH为1.5--2.8,铝离子和亚铁离子开始沉淀的溶液pH大于3,所以调节溶液的pH约为3,可以使铁离子全部沉淀,铝离子不沉淀分离;
故答案为:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀;
(4)一定条件下,MnO4-可与Mn2+反应生成MnO2
①向Ⅲ的沉淀中加入浓HCl并加热,二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,生成的氯气是黄绿色气体,能说明沉淀中存在MnO2的现象是生成黄绿色气体;
故答案为:生成黄绿色气体;
②MnO4-可与Mn2+反应生成MnO2,过滤除去,所以可以利用MnSO4的溶液和高锰酸钾溶液反应生成二氧化锰,把过量高锰酸根离子除去;
故答案为:除去过量的MnO4-.
点评 本题考查了镁、铝、铁及其化合物性质的应用,主要是混合物分离的方法和实验设计,加入氧化剂氧化亚铁离子,调节溶液PH是沉淀分离是解题的关键,题目难度中等.

 小夫子全能检测系列答案
小夫子全能检测系列答案| A. | 烷烃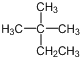 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 | |
| B. | 甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种 | |
| C. | 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,其原理相同 | |
| D. | 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |
实验名称:氯水的性质实验
实验目的:验证氯水:①有酸性,②有漂白性(氧化性),③存在Cl-
实验用品:主要仪器用品:试管、胶头滴管.
选用试剂:新制的饱和氯水、NaOH溶液、滴有酚酞的NaOH溶液,请添加其他必需试剂:品红溶液、硝酸银溶液、稀硝酸.
实验步骤:依次验证氯水的上述三项化学性质.
实验记录表:
| 步骤编号 | 操作过程 | 实验现象 | 实验结论 |
| ① | 氯水有酸性 | ||
| ② | 氯水有漂白性 | ||
| ③ | 氯水中存在Cl- |
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |
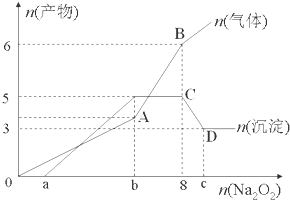
(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)a=1,b=7,c=9.
(3)写出下列离子方程式:
AB段2Na2O2+2H2O=4Na++4OH-+O2↑、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
CD段Al(OH)3+OH-=AlO2-+2H2O.
| A. | HCO3-→CO2 | B. | MnO4-→Mn2+ | C. | FeO→Fe3O4 | D. | Cl-→Cl2 |
| A. |  向氯化铝溶液中加入过量的氨水 | |
| B. | 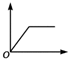 向饱和石灰水中通入过量的CO2气体 | |
| C. |  向MgCl2、AlCl3的混合液中逐滴加入NaOH溶液至过量 | |
| D. | 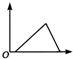 向含少量NaOH的偏铝酸钠溶液中通入过量的HCl气体 |
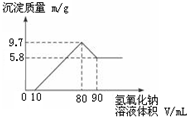 将一定质量的镁铝合金投入200mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol•L-1的NaOH溶液,生成的沉淀跟加入NaOH溶液体积的关系如图.
将一定质量的镁铝合金投入200mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol•L-1的NaOH溶液,生成的沉淀跟加入NaOH溶液体积的关系如图.
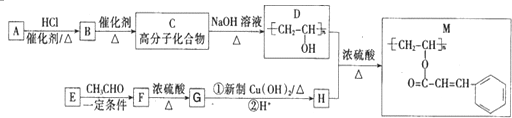
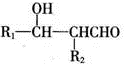
 .
. ;H的顺式结构简式为
;H的顺式结构简式为 .
. (任写一种).
(任写一种).