8.若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的化学方程式填入下表的空白处:
| 物质(杂质) | 试剂 | 有关化学方程式 |
| SiO2(Al2O3) | ||
| FeCl2(FeCl3) |
6.下列反应的离子方程式正确的是( )
| A. | .碳酸氢钙溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O | |
| C. | Na与H2O反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
0 153761 153769 153775 153779 153785 153787 153791 153797 153799 153805 153811 153815 153817 153821 153827 153829 153835 153839 153841 153845 153847 153851 153853 153855 153856 153857 153859 153860 153861 153863 153865 153869 153871 153875 153877 153881 153887 153889 153895 153899 153901 153905 153911 153917 153919 153925 153929 153931 153937 153941 153947 153955 203614
| A. | 等质量的二氧化硫和氨气,前者体积大 | |
| B. | 标况下22.4升 HCl通入水中溶液中含氯化氢分子为0.1 mol | |
| C. | 任何条件下相同物质的量的两种气体含有相同数目的分子 | |
| D. | 标况下2 molH2的摩尔质量是4g/mol |
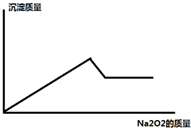 某溶液中,可能含有Al3+、Fe3+、K+、Mg2+、Fe2+、Cu2+中的一种或几种,现加入过氧化钠只产生无色无味的气体 并同时析出白色沉淀,加入过氧化钠的量与产生沉淀的量之间的关系如图
某溶液中,可能含有Al3+、Fe3+、K+、Mg2+、Fe2+、Cu2+中的一种或几种,现加入过氧化钠只产生无色无味的气体 并同时析出白色沉淀,加入过氧化钠的量与产生沉淀的量之间的关系如图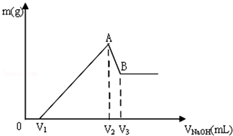 将Mg、Al组成的混合物共0.1mol溶于100mL 3mol/LHCl溶液中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V的变化如图所示:
将Mg、Al组成的混合物共0.1mol溶于100mL 3mol/LHCl溶液中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V的变化如图所示: