题目内容
10.如图是某同学设计的制取氯气以及验证氯气的性质的实验,回答下列问题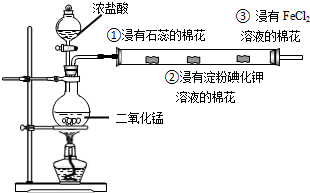
(1)该同学制取氯气的反应原理是:MnO2+4HCl(浓)$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O(写化学方程式).
(2)实验过程中②处观察到的现象是溶液变蓝说明氯气具有的性质是氧化性.
(3)该实验操作的不足之处是缺少尾气吸收装置
(4)实验室用MnO2和浓盐酸制取Cl2时,有14.6g氯化氢被氧化,所得Cl2全部用NaOH溶液吸收,生成NaClO的物质的量是0.2 moi.
分析 (1)浓盐酸与二氧化锰在加热条件下反应生成氯气、氯化锰和水;
(2)氯气具有强的氧化性,能够氧化碘化钾生成单质碘,碘遇到淀粉变蓝;
(3)氯气有毒,直接排放能够引起空气污染,应进行尾气处理;
(4)被氧化的HCl生成氯气,根据氯原子守恒计算氯气物质的量,依据方程式:Cl2+2NaOH=NaCl+NaClO+H2O,计算解答.
解答 解:(1)浓盐酸与二氧化锰在加热条件下反应生成氯气、氯化锰和水,化学方程式:MnO2+4HCl(浓) $\frac{\underline{\;加热\;}}{\;}$ MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓) $\frac{\underline{\;加热\;}}{\;}$ MnCl2+Cl2↑+2H2O;
(2)氯气具有强的氧化性,能够氧化碘化钾生成单质碘,碘遇到淀粉变蓝,故答案为:溶液变蓝;氧化性;
(3)氯气有毒,直接排放能够引起空气污染,应进行尾气处理,所以实验不足之处是:缺少尾气吸收装置;
故答案为:缺少尾气吸收装置;
(4)14.6g HCl被氧化生成氯气,由氯原子守恒可知n(Cl2)=$\frac{14.6g}{36.5g/mol}$×$\frac{1}{2}$=0.2mol,
依据方程式得:
Cl2+2NaOH=NaCl+NaClO+H2O,
1 1
0.2mol n
解得n=0.2mol.
故答案为:0.2.
点评 本题通过氯气的实验室制备考查了氯气制备原理、方程式的书写、有关方程式的计算、氯气的性质,题目难度不大,掌握基础是解题关键.

练习册系列答案
相关题目
8.某元素X,它的原子最外层电子数是次层电子数的3倍,则X在周期表中位于( )
| A. | 第三周期 | B. | 第二周期 | C. | ⅣA族 | D. | ⅤA族 |
18.通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列化学实验现象与结论对应完全正确的是( )
| 化学实验现象 | 解释与结论 | |
| A | 钠与水反应时浮在水面上 | 钠与水生成的气体托举钠浮在水面上 |
| B | 铁与氯气反应剧烈燃烧产生红棕色的烟 | 产物为红棕色小颗粒,燃烧不一定需要氧气 |
| C | 氯水呈黄绿色 | 氯气与水反应生成了黄绿色物质 |
| D | 氢气在氯气中燃烧时瓶口有白雾 | 氯气逸出结合空气中的水蒸气而呈白雾状 |
| A. | A | B. | B | C. | C | D. | D |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 等质量的二氧化硫和氨气,前者体积大 | |
| B. | 标况下22.4升 HCl通入水中溶液中含氯化氢分子为0.1 mol | |
| C. | 任何条件下相同物质的量的两种气体含有相同数目的分子 | |
| D. | 标况下2 molH2的摩尔质量是4g/mol |
15.在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A. | NH4++2H2O?NH3•H2O+H3O+ | B. | HCO3-+H2O?H3O++CO32- | ||
| C. | HS-+H+═H2S | D. | Cl2+H2O?H++Cl-+HClO |
2.V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成.下列说法正确的是( )
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为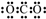 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的白烟为离子化合物,只含有离子键 |
20. 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H,如表所列数据是该反应在不同温度下的化学平衡常数(K).
①根据表中数据可判断△H<0 (填“>”、“=”或“<”),此反应较低(填“较高”或“较低”)温度下有利于该反应自发进行.
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中:
请完成此实验条件A:150℃,D:5.
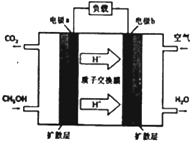
(2)甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图:
①b电极为正 极,a电极的电极反应式为:H2O+CH3OH-6e-=CO2+6H+.
②当电池消耗22.4LO2(标况下)时,消耗的甲醇的质量为$\frac{64}{3}$g.
 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H,如表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中:
请完成此实验条件A:150℃,D:5.
| 实验编号 | T(℃) | $\frac{n(CO)}{n({H}_{2})}$ | P(MPa) |
| 1 | 150 | $\frac{1}{3}$ | 0.1 |
| 2 | A | B | D |
| 3 | 350 | C | 5 |
①b电极为正 极,a电极的电极反应式为:H2O+CH3OH-6e-=CO2+6H+.
②当电池消耗22.4LO2(标况下)时,消耗的甲醇的质量为$\frac{64}{3}$g.