题目内容
6.下列反应的离子方程式正确的是( )| A. | .碳酸氢钙溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O | |
| C. | Na与H2O反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
分析 A.二者反应生成碳酸钙和水;
B.氢氧化铝与盐酸反应生成氯化铝和水;
C.电荷不守恒;
D.醋酸为弱酸应保留化学式.
解答 解:A.碳酸氢钙溶液中加入少量氢氧化钠溶液,离子方程式:Ca2++HCO3-+OH-═CaCO3+H2O,故A错误;
B.胃舒平治疗胃酸过多,离子方程式:Al(OH)3+3H+═Al3++3H2O,故B正确;
C.Na与H2O反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故C错误;
D.碳酸钙溶于醋酸中,离子方程式:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
相关题目
4.下列离子方程式正确的是( )
| A. | 向NaHSO4溶液中滴加Ba(OH)2溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 向饱和Na2CO3溶液中通入足量CO2:2Na++CO32-+CO2+H2O=2NaHCO3↓ | |
| C. | 向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液:Ca2++HCO3-+2OH-=CaCO3↓+CO32-+2H2O | |
| D. | 硫酸溶液于氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
14.中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者,青蒿素的分子式为C15H22O5,它属于有机物,易溶于乙酸、苯,可溶于乙醇、几乎不溶于水,下列说法不正确的是( )
| A. | 人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段 | |
| B. | 从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种物理变化 | |
| C. | 可以用苯把溶解在乙醇中的青蒿素萃取出来,静置分层后,下层为苯的青蒿素溶液 | |
| D. | 现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素 |
1.以下物质间的每步转化通过一步反应能实现的是( )
| A. | Al--Al2O3--Al(OH)3--NaAlO2 | B. | Fe--FeO--Fe(OH)2--Fe(OH)3 | ||
| C. | S--SO3--H2SO4--MgSO4 | D. | Na--Na2O2--Na2CO3--NaOH |
18.只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是( )
| A. | Ba(OH)2 | B. | H2SO4 | C. | NaOH | D. | Fe(OH)3胶体 |
15.下列说法不正确的是( )
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
16.下列做法不能达到实验目的是( )
| A. | 用闻气味的方法鉴别氢气和氧气 | B. | 用氯化钡溶液鉴别盐酸和稀硫酸 | ||
| C. | 观察气体颜色区别氯气和氧气 | D. | 利用丁达尔效应区别溶液和胶体 |
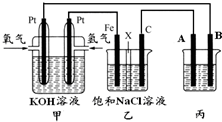 某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和电镀的原理,其中乙装置中X为阳离子交换膜.
某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和电镀的原理,其中乙装置中X为阳离子交换膜.