题目内容
8.若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的化学方程式填入下表的空白处:| 物质(杂质) | 试剂 | 有关化学方程式 |
| SiO2(Al2O3) | ||
| FeCl2(FeCl3) |
分析 氧化铝与盐酸反应,而二氧化硅与盐酸不反应;
氯化铁与Fe反应生成氯化亚铁,以此来解答.
解答 解:氧化铝与盐酸反应,而二氧化硅与盐酸不反应,则除杂试剂为盐酸,发生反应为Al2O3+6HCl=2AlCl3+3H2O;
氯化铁与Fe反应生成氯化亚铁,除杂试剂为铁,发生反应为Fe+2FeCl3=3FeCl2,
故答案为:
| 物质(杂质) | 试剂 | 有关化学方程式 |
| SiO2(Al2O3) | 盐酸 | Al2O3+6HCl=2AlCl3+3H2O |
| FeCl2(FeCl3) | 铁 | Fe+2FeCl3=3FeCl2 |
点评 本题考查混合物分离提纯,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握物质的性质、发生的反应及元素化合物知识为解答该题的关键,难度不大.

练习册系列答案
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
6.下列离子在pH=2的溶液中能大量共存,且为无色溶液的是( )
| A. | NH4+、Cl-、K+、NO3- | B. | CO32-、Na+、Cl-、K+ | ||
| C. | Fe3+、Mg2+、NO3-、Cl- | D. | Na+、Ag+、NO3-、Cl- |
19.图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法正确的是( )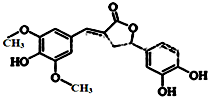

| A. | 分子中含有三种官能团 | |
| B. | 1 mol 该化合物最多能与6 mol NaOH 反应 | |
| C. | 1 mol 该化合物最多能与含4 molBr2的浓溴水反应 | |
| D. | 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2 |
16.在无色透明强酸性溶液中,能大量共存的离子组是( )
| A. | K+、Ca2+、HCO3-、SO42- | B. | Cl-、NO3-、Fe2+、K+ | ||
| C. | Na+、OH-、MnO4-、Ba2+ | D. | K+、Mg2+、NO3-、SO42- |
20.菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷.下列说法不正确的是( )
| A. | 五价砷在维生素C作用下发生了还原反应 | |
| B. | “两者同食”发生的反应中维生素C作还原剂 | |
| C. | 河虾中含有的五价砷,没有毒性 | |
| D. | 毒药砒霜是含砷的氧化物,可以推测砒霜中所含的砷元素化合价为+5 |
17.NaH中的氢元素为-1价,它可用作生氢剂,反应的化学方程式是NaH+H2O═NaOH+H2↑.则下列说法正确的是( )
| A. | NaOH是氧化产物 | |
| B. | 当1molNaH发生反应时,该反应转移电子的物质的量为2mol | |
| C. | NaH为还原剂 | |
| D. | H2O既是还原剂又是氧化剂 |
18.一份质量为2g的合金,与足量的盐酸完全反应生成0.1g H2,则该合金可能是( )
| A. | Fe-Zn合金 | B. | Fe-Cu合金 | C. | Fe-Mg合金 | D. | Mg-Al合金 |
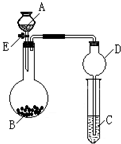 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题: