5.下表为元素周期表前四周期的一部分,其中的编号代表对应的元素.
(1)表中元素⑩的价层电子排布图为 ;
;
(2)由元素⑩⑤⑦组成一种原子个数比为1:5:5的配位化合物,该物质常温下呈液态,熔点为20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断:该化合物的晶体中存在的作用力有BDF;
A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键
(3)元素⑤⑥⑦⑧的第一电离能由大到小的顺序是(用元素符号表示)F>N>O>C,元素①分别与⑤⑥⑦形成最简单的常见化合物分子甲、乙和丙.下列有关叙述不正确的有CD;
A.甲、乙和丙分子的空间构型分别为正四面体型、三角锥形、V型
B.甲、乙和丙分子中,中心原子的杂化类型均为sp3
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(4)元素①④⑦能形成原子个数比为3:1:3的一元含氧酸,该酸能溶于水且能促进水的电离,此过程生成的离子中④原子满足最外层8电子的稳定结构,请写出该酸溶于水时的电离方程式H3BO3+H2O?[B(OH)4]-+H+;
(5)②、③均是金属元素,可分别与⑦形成同种类型的晶体Ⅰ和晶体Ⅱ,二者熔点如表所示.试指出后者熔点比前者高出许多的原因:BeO、Li2O均形成离子晶体,Be2+离子所带电荷比Li+离子的高,且半径比Li+离子的小,故BeO的晶格能比Li2O的晶格能大;
(6)元素⑤可形成多种单质,其中石墨是良好的电极材料.石墨嵌入化合物有许多独特的性质,某钾(•)的石墨嵌入化合物层状结构如图所示,该层化合物的化学式为KC12.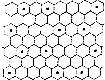
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||
| ⑨ | ⑩ |
 ;
;(2)由元素⑩⑤⑦组成一种原子个数比为1:5:5的配位化合物,该物质常温下呈液态,熔点为20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断:该化合物的晶体中存在的作用力有BDF;
A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键
(3)元素⑤⑥⑦⑧的第一电离能由大到小的顺序是(用元素符号表示)F>N>O>C,元素①分别与⑤⑥⑦形成最简单的常见化合物分子甲、乙和丙.下列有关叙述不正确的有CD;
A.甲、乙和丙分子的空间构型分别为正四面体型、三角锥形、V型
B.甲、乙和丙分子中,中心原子的杂化类型均为sp3
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(4)元素①④⑦能形成原子个数比为3:1:3的一元含氧酸,该酸能溶于水且能促进水的电离,此过程生成的离子中④原子满足最外层8电子的稳定结构,请写出该酸溶于水时的电离方程式H3BO3+H2O?[B(OH)4]-+H+;
(5)②、③均是金属元素,可分别与⑦形成同种类型的晶体Ⅰ和晶体Ⅱ,二者熔点如表所示.试指出后者熔点比前者高出许多的原因:BeO、Li2O均形成离子晶体,Be2+离子所带电荷比Li+离子的高,且半径比Li+离子的小,故BeO的晶格能比Li2O的晶格能大;
| 晶体Ⅰ | 晶体Ⅱ | |
| 熔点/K | 1840 | 2803 |

2.下表是Fe2+、Fe3+、Zn2+被OH-完全沉淀时溶液的pH.某硫酸锌酸性溶液中含有少量Fe2+、Fe3+杂质,为制得纯净的ZnSO4,应加入的试剂是( )
| 金属离子 | Fe2+ | Fe3+ | Zn2+ |
| 完全沉淀时的pH | 7.7 | 4.5 | 6.5 |
| A. | H2O2、ZnO | B. | 氨水 | C. | KMnO4、ZnCO3 | D. | NaOH溶液 |
1.一定条件下,下列说法正确的是( )
| A. | 向氨水中加入氯化铵固体,会使溶液的pH减小 | |
| B. | 常温时,向CaCO3的饱和溶液中加入Na2CO3固体,则CaCO3的溶度积常数增大 | |
| C. | 常温时,把pH=1的醋酸溶液稀释10倍后,其pH大于2 | |
| D. | 稀释Na2CO3溶液,溶液中c(OH-)增大 |
20.在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应,H2(g)+I2(g)?2HI(g)△H<0,下列说法正确的是( )
| A. | 保持容器容积不变,向其加入1molH2(g),反应速率一定加快 | |
| B. | 保持容器容积不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| C. | 保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| D. | 保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),反应速率一定加快 |
19.下列除去杂质的方法,正确的是( )
| A. | 除去乙烷中少量的乙烯:催化剂条件下通入H2 | |
| B. | 乙醇中含有乙酸杂质:加入 碳酸钠溶液,分液 | |
| C. | FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 | |
| D. | CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
18.下列实验中制取气体的药品和装置图正确的是( )
| A. |  制NH3 | B. | 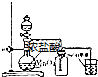 制Cl2 | C. | 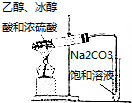 制乙酸乙酯 | D. | 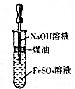 制Fe(OH)2 |
17.化学与人类生成、生活、社会可持续发展密切相关.下列说法不正确的是( )
| A. | 将“地沟油”反应改性制成“生物柴油”,代替柴油作为内燃机燃料的做法符合“绿色化学”的理念 | |
| B. | 红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 | |
| C. | 科学家推测月尘[即月球上直径小于10微米(1μm=1×10-6m)的浮尘]是“玉兔号”出现控制异常情况的主要原因,月尘在空气中形成的分散系不属于胶体 | |
| D. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
16.用一种试剂就可以将NaOH、KSCN、AgNO3、Na2SO4四种无色溶液一一鉴别出来,这种试剂是( )
0 153704 153712 153718 153722 153728 153730 153734 153740 153742 153748 153754 153758 153760 153764 153770 153772 153778 153782 153784 153788 153790 153794 153796 153798 153799 153800 153802 153803 153804 153806 153808 153812 153814 153818 153820 153824 153830 153832 153838 153842 153844 153848 153854 153860 153862 153868 153872 153874 153880 153884 153890 153898 203614
| A. | 稀盐酸 | B. | FeCl3 | C. | Fe(NO3)3 | D. | BaCl2 |
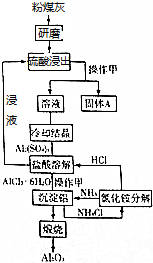 我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示:
我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示:
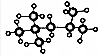 ,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;
,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;