题目内容
19.下列除去杂质的方法,正确的是( )| A. | 除去乙烷中少量的乙烯:催化剂条件下通入H2 | |
| B. | 乙醇中含有乙酸杂质:加入 碳酸钠溶液,分液 | |
| C. | FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 | |
| D. | CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
分析 A.乙烯与氢气加成,易引入新杂质氢气;
B.乙酸与碳酸钠反应后,与乙醇不分层;
C.Fe与氯化铁、氯化铜均反应;
D.HCl与饱和碳酸氢钠反应生成二氧化碳.
解答 解:A.乙烯与氢气加成,易引入新杂质氢气,不能除杂,应选溴水、洗气除杂,故A错误;
B.乙酸与碳酸钠反应后,与乙醇不分层,不能分液,应利用蒸馏法分离,故B错误;
C.Fe与氯化铁、氯化铜均反应,不能除杂,应选氧化铁促进铜离子水解,故C错误;
D.HCl与饱和碳酸氢钠反应生成二氧化碳,则通入饱和NaHCO3溶液,洗气可除杂,故D正确;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
15.短周期元素A、B、C、D中,A既可以形成阳离子又能形成简单阴离子,且非金属性A<D,B、C、D三种元素在同一周期且最外层电子数之和为11,B、D最外层电子数之和是B、C最外层电子数之和的2倍,B的最高价氧化物的水化物在短周期中碱性最强,下列判断不正确的是( )
| A. | 离子半径:D>B>C>A | |
| B. | 金属性:B>C | |
| C. | A、D最高化合价与最低化合价的代数和分别为0和6 | |
| D. | B和A、C形成的氧化物均不反应 |
10.下列反应的离子方程式书写正确的是( )
| A. | 铁粉与稀盐酸的反应:Fe+2H+═Fe2++H2↑ | |
| B. | 硫酸铝溶液与氨水的反应:Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化铜与稀硫酸的反应:OH-+H+═H2O | |
| D. | 钠与水的反应:Na+2H2O═Na++2OH-+H2↑ |
7.产物主要是Fe2O3的反应是( )
| A. | 铁在纯氧中燃烧 | B. | 红热的铁和水蒸气反应 | ||
| C. | Fe2(CO4)3与氨水混合 | D. | 灼烧氢氧化铁固体 |
14.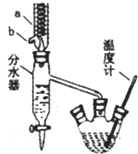 苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
(1)制备粗产品:如图所示装置中,于50mL圆底烧瓶中加人8.0g苯甲酸(Mr=122)、20mL乙醇(Mr=46,密度0.79g?cm-3)、15mL环己烷、3mL浓硫酸,摇匀,加沸石.在分水器上加水,接通冷凝水,水浴回流约2h,反应基本完成.记录体积,继续蒸出多余环己烷和醇(从分水器中放出).
(2)粗产品纯化:加水30ml.,分批加人固体NaHCO3,分液,然后水层用20mL石油醚分两次萃取.合并有机层,用无水硫酸镁干燥.回收石油醚,加热精馏,收集210一213℃馏分.
相关数据如表:
请根据以上信息和装置图回答下述实验室制备有关问题:
(1)写出制备苯甲酸乙醋反应的化学方程式 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O仪器a的名称冷凝管,b口的作用为出水口,
+H2O仪器a的名称冷凝管,b口的作用为出水口,
(2)请说出在本实验中可以采取的能提高笨甲酸乙酸产率的方法加入环已烷形成水-乙醇-环已烷三元共沸物分离出反应过程中生成的水,或加过量的乙醇,或使用分液器及时分离子出生成的水等(写出任意一种即可).
(3)如何利用实验现象判断反应已基本完成加热回流至分水器中水位不再上升
(4)固体NaHCO.的作用中和硫酸和未反应的苯甲酸,加人固体NaHCO3时的实验操作所用到的主要玻璃仪器为分液漏斗.
(5)经精馏得210-213℃馏分7.0mL,则实验中苯甲酸乙脂的产率为73.7%.
 苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:(1)制备粗产品:如图所示装置中,于50mL圆底烧瓶中加人8.0g苯甲酸(Mr=122)、20mL乙醇(Mr=46,密度0.79g?cm-3)、15mL环己烷、3mL浓硫酸,摇匀,加沸石.在分水器上加水,接通冷凝水,水浴回流约2h,反应基本完成.记录体积,继续蒸出多余环己烷和醇(从分水器中放出).
(2)粗产品纯化:加水30ml.,分批加人固体NaHCO3,分液,然后水层用20mL石油醚分两次萃取.合并有机层,用无水硫酸镁干燥.回收石油醚,加热精馏,收集210一213℃馏分.
相关数据如表:
| 沸点(℃,1atm) | ||||||
| 苯甲酸 | 苯甲酸乙酯 | 石油醚 | 水 | 乙醇 | 环己烷 | 共沸物(环已烷-水-乙醇) |
| 249 | 212.6 | 40-80 | 100 | 78.3 | 80.75 | 62.6 |
(1)写出制备苯甲酸乙醋反应的化学方程式
 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O仪器a的名称冷凝管,b口的作用为出水口,
+H2O仪器a的名称冷凝管,b口的作用为出水口,(2)请说出在本实验中可以采取的能提高笨甲酸乙酸产率的方法加入环已烷形成水-乙醇-环已烷三元共沸物分离出反应过程中生成的水,或加过量的乙醇,或使用分液器及时分离子出生成的水等(写出任意一种即可).
(3)如何利用实验现象判断反应已基本完成加热回流至分水器中水位不再上升
(4)固体NaHCO.的作用中和硫酸和未反应的苯甲酸,加人固体NaHCO3时的实验操作所用到的主要玻璃仪器为分液漏斗.
(5)经精馏得210-213℃馏分7.0mL,则实验中苯甲酸乙脂的产率为73.7%.
11.漂粉精可由Cl2通入消石灰中制备,漂粉精的有效成分是( )
| A. | CaCl2 | B. | Ca(ClO)2 | C. | Ca(OH)2 | D. | CaCO3 |
8.下列说法不正确的是( )
| A. | 氢处于第一周期 | B. | 氯处于第ⅦA族 | ||
| C. | 硅与碳处于同一主族 | D. | 第三周期元素全部是金属元素 |
9.化学与环境、材料、信息、能源关系密切,下列说法正确的是( )
| A. | 氟利昂(CCl2F2)会破坏大气臭氧层从而导致“温室效应” | |
| B. | 开发高效氢能、太阳能灯新能源汽车,可以减缓城市机动车尾气污染 | |
| C. | PM2.5是指大气中直径接近2.5×10-6m的颗粒物,它分散在空气中形成胶体 | |
| D. | 海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |
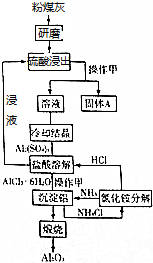 我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示:
我国煤炭丰富、电离偏紧的资源特征决定了在今后相当长一段时间内,火力发电仍将在电力工业中占据重要地位.粉煤灰是火电厂排出的主要固体废物.其中粉煤灰中主要含有SiO2、Al2O3、CaO等.一种利用粉煤灰制取氧化铝的工艺流程如图所示: