1.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1molCH5+与1molNH2-所含电子数均为10NA | |
| B. | 60gSiO2晶体中所含[SiO4]四面体数为0.5NA | |
| C. | 25℃,pH=10的Na2CO3溶液中所含OH-数为1×10-4NA | |
| D. | 标准状况下,22.4LCO、NO混合气体中所含氧原子数为2NA |
20.下列物质的分子热稳定性最好的是( )
| A. | CH4 | B. | NH3 | C. | H2O | D. | HF |
19.今有原子序数依次培大的A.B、C、D、E、F六种元素.已知A、C、E三元素原子的最外层共有10个电子.且这三种元素的最高价氧化物对应的水化物之间,两两皆能反应且均能生成盐和水.D和F各有如下表的电子层结构.
按要求填空:
(1)各元素的元素符号分别为BMg,ES,FCl;
(2)试写出A、C最高价氧化物对应的水化物之间反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O
(3)D、E氢化物的稳定性:H2S>SiH4
(4)试写出A、B、E、F形成的简单离子半径由小到大的顺序:S2->Cl->Na+>Mg2+.
| 元素 | 最外层电子数 | 次外层电子数 |
| D | x | x+4 |
| F | x+3 | x+4 |
(1)各元素的元素符号分别为BMg,ES,FCl;
(2)试写出A、C最高价氧化物对应的水化物之间反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O
(3)D、E氢化物的稳定性:H2S>SiH4
(4)试写出A、B、E、F形成的简单离子半径由小到大的顺序:S2->Cl->Na+>Mg2+.
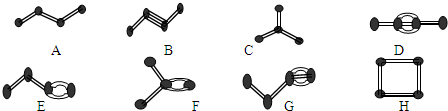
18.某有机物分子式为C3H4,仅从碳原子的连接形式和价键(单键、双键、三键)来讨论.其同分异构体有( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
17.下列卤族元素中.没有正化合价的元素是( )
| A. | F | B. | Cl | C. | Br | D. | I |
16.18g碳单质与标准状况下22.4L O2反应放出热量是Q1kJ,已知由碳单质生成1mol CO2气体放热Q2 kJ.下列说法不正确的是( )
| A. | 由碳燃烧生成CO的热化学方程式是C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=(Q1-0.5Q2)kJ/mol | |
| B. | 由碳燃烧生成1mol CO放出的热量是(Q1-0.5Q2)kJ | |
| C. | 由碳燃烧生成CO的热化学方程式是2C(s)+O2(g)═2CO(g)△H=(Q2-2Q1)kJ/mol | |
| D. | 碳和CO2反应的热化学方程式是C(s)+CO2(g)═2CO(g)△H=(2Q2-2Q1)kJ/mol |
15.短周期元素A、B、C、D中,A既可以形成阳离子又能形成简单阴离子,且非金属性A<D,B、C、D三种元素在同一周期且最外层电子数之和为11,B、D最外层电子数之和是B、C最外层电子数之和的2倍,B的最高价氧化物的水化物在短周期中碱性最强,下列判断不正确的是( )
0 153697 153705 153711 153715 153721 153723 153727 153733 153735 153741 153747 153751 153753 153757 153763 153765 153771 153775 153777 153781 153783 153787 153789 153791 153792 153793 153795 153796 153797 153799 153801 153805 153807 153811 153813 153817 153823 153825 153831 153835 153837 153841 153847 153853 153855 153861 153865 153867 153873 153877 153883 153891 203614
| A. | 离子半径:D>B>C>A | |
| B. | 金属性:B>C | |
| C. | A、D最高化合价与最低化合价的代数和分别为0和6 | |
| D. | B和A、C形成的氧化物均不反应 |
 根据如图的物理模型,回答问题:
根据如图的物理模型,回答问题: