题目内容
15.短周期元素A、B、C、D中,A既可以形成阳离子又能形成简单阴离子,且非金属性A<D,B、C、D三种元素在同一周期且最外层电子数之和为11,B、D最外层电子数之和是B、C最外层电子数之和的2倍,B的最高价氧化物的水化物在短周期中碱性最强,下列判断不正确的是( )| A. | 离子半径:D>B>C>A | |
| B. | 金属性:B>C | |
| C. | A、D最高化合价与最低化合价的代数和分别为0和6 | |
| D. | B和A、C形成的氧化物均不反应 |
分析 A元素的原子能形成简单阴离子,应为非金属元素,又能形成简单阳离子,只能为H元素,B的最高价氧化物的水化物在短周期中碱性最强,应为Na元素,最外层电子数为1,B、D最外层电子数之和是B、C最外层电子数之和的2倍,只有Al、Cl符合,则D为Cl,C为Al元素,结合对应元素的单质以及化合物的性质解答该题.
解答 解:A元素的原子能形成简单阴离子,应为非金属元素,又能形成简单阳离子,只能为H元素,B的最高价氧化物的水化物在短周期中碱性最强,应为Na元素,最外层电子数为1,B、D最外层电子数之和是B、C最外层电子数之和的2倍,只有Al、Cl符合,则D为Cl,C为Al元素,
A.D为Cl,B为Na,C为Al,钠和铝的阳离子具有相同的电子层数,钠离子半径较小,氯离子比钠离子、铝离子多一个电子层,氢离子半径最小,则有D>B>C>A,故A正确;
B.同周期元素从左到右金属性逐渐减小,则金属性:B>C,故B正确;
C.A最高化合价为+1价,最低化合价为-1价,D最高化合价为+7价,最低化合价为-1价,则代数和分别为0和6,故C正确;
D.钠和水反应生成氢氧化钠和氢气,故D错误.
故选D.
点评 本题考查原子结构与元素周期律知识,为高频考点,题目难度中等,明确元素的种类为解答该题的关键,本题注意对应单质、化合物的性质,解答该题时能举出相关例子.

练习册系列答案
相关题目
6.用下列实验装置进行相应实验,设计正确且能达到实验目的是( )
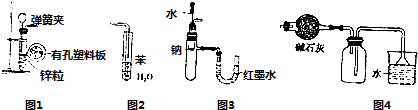

| A. | 用图1所示装置制取少量H2 | |
| B. | 用图2所示装置吸收氨气以防止倒吸 | |
| C. | 用图3所示装置验证Na和水反应的热效应 | |
| D. | 用图4所示装置可用于干燥、收集氯化氢气体 |
3.对于可逆反应mA+nB?pC正反应的反应热为△H.分别改变温度、压强、B的物质的量导致平衡常数(K)、A的转化率(a%)、A的物质的量浓度[c(A)]发生如图所示的变化.根据图中变化情况,以下结论正确的是( )
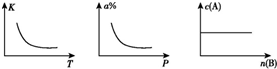

| A. | m+n<p,△H>0 A、B、C均为气体 | B. | m<p△H<0 A、C均为气体 | ||
| C. | n>p,△H>0 B、C均为气体 | D. | m>p,△H<0 A、C均为气体 |
20.下列物质的分子热稳定性最好的是( )
| A. | CH4 | B. | NH3 | C. | H2O | D. | HF |
1. Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当改变条件,再次达到平衡时,下列有关叙述不正确的是( )
 Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
| A. | 若升高温度到某一温度,再次达到平衡时,相应点可能分别是A、E | |
| B. | 若再次充入a mol HI,则达到平衡时,相应点的横坐标值不变,纵坐标值增大 | |
| C. | 若改变的条件是增大压强,再次达到平衡时,相应点与改变条件前相同 | |
| D. | 若改变的条件是使用催化剂,再次达到平衡时,相应点与改变条件前不同 |
18.设NA表示阿伏伽德罗常数的值,下列说法正确的是(相对原子质量:H-1,N-14)( )
| A. | 标准状况下,22.4LHCl溶于水后溶液中含有NA个HCl分子 | |
| B. | 常温常压下,33.6LCl2中含有1.5NA个Cl2分子 | |
| C. | 1.8g的NH4+离子中含有NA个电子 | |
| D. | 将0.1mol氯化铝溶于1L水中,所得溶液含有0.1NAAl3+ |
19.下列除去杂质的方法,正确的是( )
| A. | 除去乙烷中少量的乙烯:催化剂条件下通入H2 | |
| B. | 乙醇中含有乙酸杂质:加入 碳酸钠溶液,分液 | |
| C. | FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 | |
| D. | CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
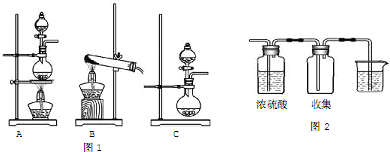
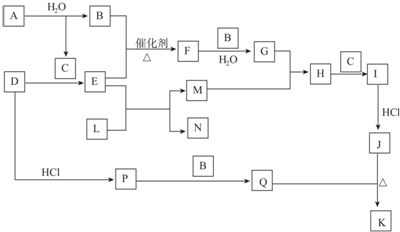
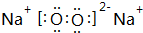 ,D的化学式(NH4)2S.
,D的化学式(NH4)2S.