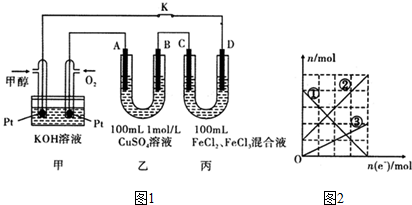
10.高氯酸钾广泛用于火箭及热电池等领域.实验室制取高氯酸钾的步骤为:
称取一定质量的KCl、NaClO4,溶解后混合,经冷却、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到,有关物质溶解度与温度的关系如下表:
(1)写出实验室制取高氯酸钾的化学方程式NaClO4+KCl═KClO4↓+NaCl;用蒸馏水多次洗涤晶体的目的是尽可能除去溶解度较大的杂质.
(2)热电池是以熔盐作电解质,利用热源使其溶化而激活得一次储备电池.Li/FeS2热电池工作时,Li转变为硫化锂,FeS2转变为铁,该电池工作时,电池总反应为FeS2+4Li═Fe+2Li2S.
(3)Fe和KClO4反应放出的热量能为熔融盐电池提供550-660℃的温度,使低熔点盐熔化导电,从而激活电池,其供热原理为:KClO4 (s)+4Fe(s)═KCl (s)+4FeO(s),△H<0.
①600℃时FeO可部分分解生成Fe3O4,写出有关的化学方程式4FeO=Fe3O4+Fe.
②称取一定质量上述加热材料反应后的混合物(假定只含氯化钾一种钾盐)于烧杯中,用蒸馏水充分洗涤、过滤、干燥,固体质量减少了0.43g,在固体中继续加入过量的稀硫酸,微热让其充分反应,固体完全溶解得到的溶液中加入过量的NaOH溶液,经过滤、洗净、干燥,再在空气中充分灼烧得6.0 g棕色固体.求该加热材料反应前,铁和高氯酸钾的质量.(写出计算过程,结果保留2位有效数字)该加热材料反应前铁和高氯酸钾的质量分别为4.2g、0.80g.
称取一定质量的KCl、NaClO4,溶解后混合,经冷却、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到,有关物质溶解度与温度的关系如下表:
| 温度 溶解度 化学式 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| KClO4 | 0.76 | 1.06 | 1.68 | 2.56 | 3.73 |
| KCl | 28 | 31.2 | 34.2 | 37.2 | 40.1 |
| NaClO4 | 167 | 183 | 201 | 222 | 245 |
(2)热电池是以熔盐作电解质,利用热源使其溶化而激活得一次储备电池.Li/FeS2热电池工作时,Li转变为硫化锂,FeS2转变为铁,该电池工作时,电池总反应为FeS2+4Li═Fe+2Li2S.
(3)Fe和KClO4反应放出的热量能为熔融盐电池提供550-660℃的温度,使低熔点盐熔化导电,从而激活电池,其供热原理为:KClO4 (s)+4Fe(s)═KCl (s)+4FeO(s),△H<0.
①600℃时FeO可部分分解生成Fe3O4,写出有关的化学方程式4FeO=Fe3O4+Fe.
②称取一定质量上述加热材料反应后的混合物(假定只含氯化钾一种钾盐)于烧杯中,用蒸馏水充分洗涤、过滤、干燥,固体质量减少了0.43g,在固体中继续加入过量的稀硫酸,微热让其充分反应,固体完全溶解得到的溶液中加入过量的NaOH溶液,经过滤、洗净、干燥,再在空气中充分灼烧得6.0 g棕色固体.求该加热材料反应前,铁和高氯酸钾的质量.(写出计算过程,结果保留2位有效数字)该加热材料反应前铁和高氯酸钾的质量分别为4.2g、0.80g.
7.为证明某可溶性一元酸(HX)是弱酸.有如下实验方案,其中不合理的是( )
0 153692 153700 153706 153710 153716 153718 153722 153728 153730 153736 153742 153746 153748 153752 153758 153760 153766 153770 153772 153776 153778 153782 153784 153786 153787 153788 153790 153791 153792 153794 153796 153800 153802 153806 153808 153812 153818 153820 153826 153830 153832 153836 153842 153848 153850 153856 153860 153862 153868 153872 153878 153886 203614
| A. | 将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 | |
| B. | 室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 | |
| C. | 室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 | |
| D. | 相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |


 (1)已知1molSO2(g)生成1molSO3(g)的能量变化如图所示,回答下列问题:
(1)已知1molSO2(g)生成1molSO3(g)的能量变化如图所示,回答下列问题:
 ;写出A分子中官能团的名称羟基、羧基;
;写出A分子中官能团的名称羟基、羧基; ;
;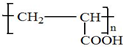 .
.