3.下列离子组在溶液中能大量共存的是( )
| A. | H+、Fe2+、Cl-、NO3- | B. | K+、H+、CO32-、HCO3- | ||
| C. | Ca2+、Ba2+、Cl-、HCO3- | D. | Na+、Ba2+、HCO3-、OH- |
2.一定条件下,反应N2(g)+3H2(g)?2NH3(g)在10L的密闭容器中进行,测得2min内N2的物质的量由20mol减小到8mol,则2min内用NH3表示的反应速率为( )
| A. | 1.2mol/(L•min) | B. | 6.0mol/(L•min) | C. | 0.6mol/(L•min) | D. | 0.4mol/(L•min) |
1.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的金属性最强,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述不正确的是( )
| A. | X与Y能形成两种常见的气态化合物 | |
| B. | 原子半径的大小顺序:r(Z)>r(R)>r(X)>r(Y) | |
| C. | X、Z分别与R形成的化合物中化学键类型不同 | |
| D. | 含有Y、Z、R三种元素的化合物最多只有2种 |
18.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4═2PbSO4↓+2H2O,根据此反应判断下列有关该电池的说法错误的是( )
| A. | 该电池的正极板上覆盖有PbO2,负极板上覆盖有Pb | |
| B. | 该电池放电时的正极反应为PbO2(s)+4H+(aq)+SO2-4(aq)+2e-═PbSO4(s)+2H2O(l) | |
| C. | 该电池充电时,两个电极上都有PbSO4生成 | |
| D. | 用该电池电解饱和食盐水制氯气,若制得0.050molCl2,这时电池内消耗H2SO40.10mol |
17.研究性学习是综合实践活动重要的组成部分,注重培养学生的问题意识.某研究性学习小组为了验证臭氧的氧化性强于氧气,进行了下述实验,请参与探究并回答相关问题.
[实验目的]验证臭氧的氧化性强于氧气.
[实验原理]2KI+O3+H2O═2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]
①取a溶液与碘化钾溶液混合.
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上.
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等.
④观察现象并进行记录:
请根据上述实验原理、步骤及你所学的知识,回答下列问题.
(1)实验药品中的a溶液是淀粉溶液.
(2)写出在臭氧消毒柜中产生O3的化学方程式:3O2$\frac{\underline{\;通电\;}}{\;}$2O3.
(3)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是温度会影响反应速率,保持温度相同是为了消除温度不同带来的误差.
(4)从实验数据记录可以得出的结论是BCD(填序号).
A.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
B.氧气也能氧化碘化钾中的碘离子
C.O3的氧化性比O2强
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(5)在O3氧化KI的反应中,若有24g O3发生反应,则转移电子的数目为NA(或6.02×1023).
[实验目的]验证臭氧的氧化性强于氧气.
[实验原理]2KI+O3+H2O═2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]
①取a溶液与碘化钾溶液混合.
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上.
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等.
④观察现象并进行记录:
| 时间/min | 0 | 15 | 30 | 45 | 60 | 90 | 120 | |
| 滤纸的 颜色 变化 | 玻璃片(Ⅰ) 上的滤纸 | 白色 | 白色 | 灰色 | 浅蓝色 | 蓝色 | 蓝色 | 浅蓝色 |
| 玻璃片(Ⅱ) 上的滤纸 | 白色 | 白色 | 白色 | 白色 | 灰色 | 灰色 | 浅蓝色 | |
(1)实验药品中的a溶液是淀粉溶液.
(2)写出在臭氧消毒柜中产生O3的化学方程式:3O2$\frac{\underline{\;通电\;}}{\;}$2O3.
(3)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是温度会影响反应速率,保持温度相同是为了消除温度不同带来的误差.
(4)从实验数据记录可以得出的结论是BCD(填序号).
A.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
B.氧气也能氧化碘化钾中的碘离子
C.O3的氧化性比O2强
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(5)在O3氧化KI的反应中,若有24g O3发生反应,则转移电子的数目为NA(或6.02×1023).
15.利用水钴矿[主要成分为Co2O3和Co(OH)3,还有少量Fe2O3、Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如图所示:
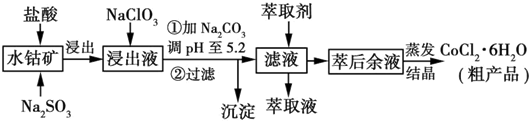
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+═2Co2++SO42-+2H2O.
(2)NaClO3的作用是将Fe2+氧化成Fe3+.
(3)加Na2CO3调pH至5.2所得沉淀为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图所示.萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B(填字母).
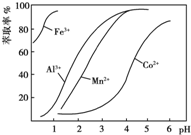
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去部分结晶水(任答一条即可).
0 153619 153627 153633 153637 153643 153645 153649 153655 153657 153663 153669 153673 153675 153679 153685 153687 153693 153697 153699 153703 153705 153709 153711 153713 153714 153715 153717 153718 153719 153721 153723 153727 153729 153733 153735 153739 153745 153747 153753 153757 153759 153763 153769 153775 153777 153783 153787 153789 153795 153799 153805 153813 203614

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将Fe2+氧化成Fe3+.
(3)加Na2CO3调pH至5.2所得沉淀为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图所示.萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B(填字母).

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去部分结晶水(任答一条即可).
 某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.
某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.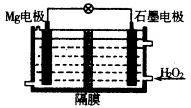 钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.
钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.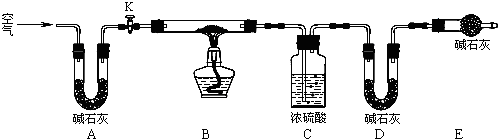
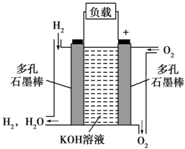 如图所示为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
如图所示为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: