题目内容
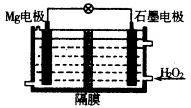
14.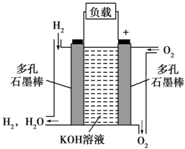 如图所示为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
如图所示为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:(1)图中通过负载的电子流动方向为向右(填“向左”或“向右”).
(2)氢氧燃料电池工作时的正极反应为2H2O+O2+4e-═4OH-,反应中若转移2mol电子,消耗H2的体积为22.4L(标准状况).
(3)为了获得氢气,除了充分利用太阳能外,工业上利用石油产品与水在催化剂作用下制取氢气.写出C3H8和H2O反应生成H2和CO的化学方程式C3H8+3H2O$\frac{\underline{催化剂}}{△}$3CO+7H2.
(4)若将此燃料电池改为直接以甲烷和氧气为原料进行工作时,正极反应为2O2+4H2O+8e-=8OH-,负极反应为CH4+10OH--8e-═CO32-+7H2O.
分析 (1)根据原电池工作原理判断电子的流向;
(2)根据反应的反应类型书写电极反应式,结合电子守恒进行计算;
(3)根据反应物、生成物、反应条件写出反应方程式;
(4)先根据反应类型确定负极上发生反应的物质,然后写出相应的电极反应式.
解答 解:(1)根据原电池工作原理,负极上失电子,电子从负极沿外电路流向正极,所以通过负载的电子流动方向是向右.
故答案为:向右;
(2)正极上氧气得电子和水生成氢氧根离子,发生还原反应,所以电极反应式为2H2O+O2+4e-═4OH-;负极上失电子和氢氧根离子反应生成水,所以电极反应式为2H2+4OH--4e-═4H2O;反应中若转移2mol电子,消耗H2的物质的量是1mol,体积是22.4L.
故答案为:2H2O+O2+4e-═4OH-;22.4;
(3)该反应中反应物是丙烷和H2O,产物是H2和CO,反应条件是高温、催化剂,所以方程式为
C3H8+3H2O$\frac{\underline{催化剂}}{△}$3CO+7H2.故答案为:C3H8+3H2O$\frac{\underline{催化剂}}{△}$3CO+7H2;
(4)负极上是燃料失电子,正极上是氧气得电子,所以负极上甲烷反应生成二氧化碳,二氧化碳是酸性氧化物,能和电解质溶液KOH反应生成盐和水,所以负极上的电极反应式为CH4+10OH--8e-═CO32-+7H2O;正极上氧气得电子和水生成氢氧根离子2O2+4H2O+8e-=8OH-;.
故答案为:2O2+4H2O+8e-=8OH-;CH4+10OH--8e-═CO32-+7H2O.
点评 本题考查了燃料电池电极反应式及电池反应方程式的书写,燃料在负极上失电子发生氧化反应,氧化剂在正极上得电子发生还原反应,书写电极反应式时要结合电解质溶液确定生成的离子.

 碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=a kJ•mol-1
②3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应:Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=0.5a+bkJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间/min 浓度/mol/L | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
T1℃时,该反应的平衡常数=0.25.
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母编号)AD
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
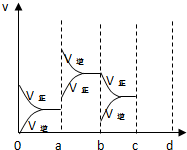
(3)如图表示在密闭容器中反应2SO2+O2?2SO3达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况.
①ab过程中改变的条件可能是:升高温度.
②bc过程中改变的条件可能是:降低产物SO3浓度.
③若增大压强时,反应速率变化情况画在c~d处.
| A. | 氯化钠的电子式: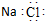 | |
| B. | 苯的结构简式:C6H6 | |
| C. | 硅的原子结构示意图: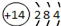 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42- |
| A. | 标准状况下,0.1NA个水分子所占的体积约是2.24 L | |
| B. | 常温常压下,11.2 L CO2中含有11NA个电子 | |
| C. | CH4的摩尔质量和NA个甲烷分子的质量相等 | |
| D. | 常温下,64gSO2气体中含有的原子数为3NA |
| A. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 | |
| B. | 金属钠着火时不能使用泡沫灭火器灭火 | |
| C. | 因为NH4Cl受热易分解,实验室应保存在棕色试剂瓶中 | |
| D. | 铁粉作食品袋内的脱氧剂,起还原作用 |
| A. | 原子一定重新组合 | B. | 一定有电子转移 | ||
| C. | 有旧键断裂和新键形成 | D. | 必然伴随着能量的变化 |
| A. | SiO2、CO2 都是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应的产物相同 | |
| C. | SO2、NO、CO2都是大气污染物,在空气中都能稳定存在 | |
| D. | HCl、HNO3都是强酸,和FeO的反应都属于复分解反应 |
 ;
; 钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.
钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.