8.下列有关银镜反应实验的说法不正确的是( )
| A. | 实验前试管先用热的烧碱溶液洗涤,再用蒸馏水洗涤 | |
| B. | 向2%的硝酸银溶液中滴入2%的稀氨水,直至产生的沉淀恰好溶解,配得银氨溶液 | |
| C. | 采用水浴加热,不能直接加热 | |
| D. | 可用浓盐酸洗去银镜 |
7.“2015.8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.已知部分弱酸的电离平衡常数如下表:
(1)根据价键规则,写出HCN的结构式是H-C≡N;
(2)下列能用于判断氮、碳两种元素非金属性强弱的是bc.(填序号)
a.气态氢化物沸点;b.最高价氧化物对应水化物酸性强弱;
c.Al2O3+N2+3C═2AlN+3CO;d.单质晶体类型;
(3)一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是CN-+H2O?HCN+OH-;通过列式计算“c(CN-)与c(HCN)”的大小K=$\frac{c(HCN)c(O{H}^{-})}{c(C{N}^{-})}$=$\frac{Kw}{Ka(HCN)}$=$\frac{1{0}^{-14}}{5×1{0}^{-10}}$,$\frac{c(HCN)}{c(C{N}^{-})}$=$\frac{2×1{0}^{-5}}{1{0}^{-5}}$=2,c(CN-)<c(HCN)判断:c(CN-)<c(HCN)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大.处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.

将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200mL倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-;乙中反应的离子方程式为2CNO-+3ClO-+2H+═N2+2CO2+3Cl-+H2O.
②乙中生成的气体除CO2、N2外还有HCl及副反应生成的Cl2等,上述实验是通过测定CO2的量来确定CN-的处理效果.丙中加入的除杂试剂是A(填标号).
(A)饱和食盐 (B)饱和NaHCO3溶液 (C)浓NaOH溶液 (D)浓硫酸
丁在实验中的作用是除去混合气体中Cl2防止对CO2测定量的影响.戊中盛有足量的石灰水,若实验后戊中共生成0.8g沉淀,则该实验中CN-被处理的百分率>80%(填“>”、“二”或“<”=).
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 ( 25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
(2)下列能用于判断氮、碳两种元素非金属性强弱的是bc.(填序号)
a.气态氢化物沸点;b.最高价氧化物对应水化物酸性强弱;
c.Al2O3+N2+3C═2AlN+3CO;d.单质晶体类型;
(3)一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是CN-+H2O?HCN+OH-;通过列式计算“c(CN-)与c(HCN)”的大小K=$\frac{c(HCN)c(O{H}^{-})}{c(C{N}^{-})}$=$\frac{Kw}{Ka(HCN)}$=$\frac{1{0}^{-14}}{5×1{0}^{-10}}$,$\frac{c(HCN)}{c(C{N}^{-})}$=$\frac{2×1{0}^{-5}}{1{0}^{-5}}$=2,c(CN-)<c(HCN)判断:c(CN-)<c(HCN)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大.处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.

将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200mL倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-;乙中反应的离子方程式为2CNO-+3ClO-+2H+═N2+2CO2+3Cl-+H2O.
②乙中生成的气体除CO2、N2外还有HCl及副反应生成的Cl2等,上述实验是通过测定CO2的量来确定CN-的处理效果.丙中加入的除杂试剂是A(填标号).
(A)饱和食盐 (B)饱和NaHCO3溶液 (C)浓NaOH溶液 (D)浓硫酸
丁在实验中的作用是除去混合气体中Cl2防止对CO2测定量的影响.戊中盛有足量的石灰水,若实验后戊中共生成0.8g沉淀,则该实验中CN-被处理的百分率>80%(填“>”、“二”或“<”=).
6.运用化学反应原理分析解答以下问题:
(1)弱酸在水溶液中存在电离平衡,部分0.1mol•L-1弱酸的电离平衡常数如表:
①当弱酸的浓度一定时,降低温度,K值变小(填“变大”“变小”或“不变”).
②下列离子方程式和有关说法错误的是ad.
a.少量的CO2通入次氯酸钠溶液中:2ClO-+H2O+CO2═2HClO+CO${\;}_{3}^{2-}$
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO${\;}_{3}^{2-}$═2HCO${\;}_{3}^{-}$+SO${\;}_{3}^{2-}$
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性.往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式:H2SeO3+2SO2+H2O=Se↓+2H2SO4.
(2)工业废水中常含有一定量的Cr2O${\;}_{7}^{2-}$和CrO${\;}_{4}^{2-}$,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放.
①在废水中存在平衡:2CrO${\;}_{4}^{2-}$(黄色)+2H+?Cr2O${\;}_{7}^{2-}$(橙色)+H2O.若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是ad.
a.平衡常数K值可以不改变
b.达到新平衡CrO${\;}_{4}^{2-}$的消耗速率等于Cr2O${\;}_{7}^{2-}$的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O${\;}_{7}^{2-}$和CrO${\;}_{4}^{2-}$最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol•L-1,溶液的pH调至4时,没有(填“有”或“没有”)沉淀产生.
(3)已知:①2CH3OH(g)?CH3OCH3(g)+H2O(g)
②CO(g)+2H2(g)?CH3OH(g)
③CO(g)+H2O(g)?CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3,则该温度下反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示).向某固定体积的密闭容器中加入3mol CO和3mol H2,充分反应后恢复至原温度,测定容器的压强为反应前的1/2,则CO的转化率为75%.
(1)弱酸在水溶液中存在电离平衡,部分0.1mol•L-1弱酸的电离平衡常数如表:
| 弱酸 | 电离平衡常数(25℃) |
| HClO | K=2.98×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| H2SO3 | K1=1.54×10-2 K2=1.02×10-7 |
②下列离子方程式和有关说法错误的是ad.
a.少量的CO2通入次氯酸钠溶液中:2ClO-+H2O+CO2═2HClO+CO${\;}_{3}^{2-}$
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO${\;}_{3}^{2-}$═2HCO${\;}_{3}^{-}$+SO${\;}_{3}^{2-}$
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性.往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式:H2SeO3+2SO2+H2O=Se↓+2H2SO4.
(2)工业废水中常含有一定量的Cr2O${\;}_{7}^{2-}$和CrO${\;}_{4}^{2-}$,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放.
①在废水中存在平衡:2CrO${\;}_{4}^{2-}$(黄色)+2H+?Cr2O${\;}_{7}^{2-}$(橙色)+H2O.若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是ad.
a.平衡常数K值可以不改变
b.达到新平衡CrO${\;}_{4}^{2-}$的消耗速率等于Cr2O${\;}_{7}^{2-}$的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O${\;}_{7}^{2-}$和CrO${\;}_{4}^{2-}$最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol•L-1,溶液的pH调至4时,没有(填“有”或“没有”)沉淀产生.
(3)已知:①2CH3OH(g)?CH3OCH3(g)+H2O(g)
②CO(g)+2H2(g)?CH3OH(g)
③CO(g)+H2O(g)?CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3,则该温度下反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示).向某固定体积的密闭容器中加入3mol CO和3mol H2,充分反应后恢复至原温度,测定容器的压强为反应前的1/2,则CO的转化率为75%.
5.为了使CH3COONa溶液中Na+的浓度与CH3COO-的浓度比为1:1,可在CH3COONa溶液中加入( )
①适量的盐酸 ②适量的NaCl ③适量的醋酸 ④适量的CH3COONa.
①适量的盐酸 ②适量的NaCl ③适量的醋酸 ④适量的CH3COONa.
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
4. 碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=a kJ•mol-1
②3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应:Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=0.5a+bkJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=0.032mol/(L•min),
T1℃时,该反应的平衡常数=0.25.
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母编号)AD
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
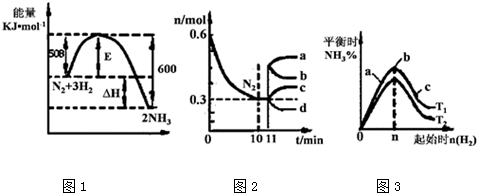
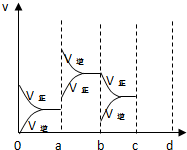
(3)如图表示在密闭容器中反应2SO2+O2?2SO3达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况.
①ab过程中改变的条件可能是:升高温度.
②bc过程中改变的条件可能是:降低产物SO3浓度.
③若增大压强时,反应速率变化情况画在c~d处.
0 153612 153620 153626 153630 153636 153638 153642 153648 153650 153656 153662 153666 153668 153672 153678 153680 153686 153690 153692 153696 153698 153702 153704 153706 153707 153708 153710 153711 153712 153714 153716 153720 153722 153726 153728 153732 153738 153740 153746 153750 153752 153756 153762 153768 153770 153776 153780 153782 153788 153792 153798 153806 203614
 碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、硼、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=a kJ•mol-1
②3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应:Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=0.5a+bkJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间/min 浓度/mol/L | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
T1℃时,该反应的平衡常数=0.25.
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母编号)AD
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)如图表示在密闭容器中反应2SO2+O2?2SO3达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况.
①ab过程中改变的条件可能是:升高温度.
②bc过程中改变的条件可能是:降低产物SO3浓度.
③若增大压强时,反应速率变化情况画在c~d处.
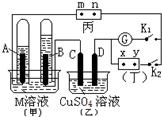 如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题:
如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题: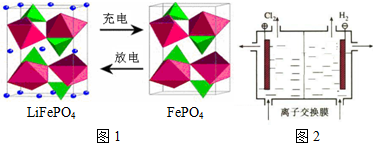
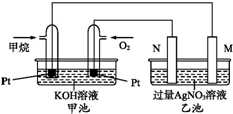 如图是一个甲烷燃料电池工作时的示意图.M、N两电极的质量相同,其中一个为银电极一个为铁电极.
如图是一个甲烷燃料电池工作时的示意图.M、N两电极的质量相同,其中一个为银电极一个为铁电极.