题目内容
10.25℃时,将0.1mol/L NaOH溶液与0.06mol/L的H2SO4溶液等体积混合(忽略混合后体积的变化),求所得溶液的pH=2.分析 根据酸的量和碱的量判断二者混合后酸剩余,计算混合后剩余氢离子浓度,进而计算pH即可.
解答 解:设两溶液体积是V,0.1mol/L NaOH溶液中氢氧根离子物质的量是0.1V,0.06mol/L的H2SO4溶液的物质的量是0.12V,混合后酸剩余,所以剩余氢离子浓度c=$\frac{0.12V-0.1V}{2V}$=0.01mol/L,即pH=2,故答案为:2.
点评 本题涉及酸碱混合后溶液pH的计算知识,属于综合知识的考查,难度中等.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
8.下列指定反应的离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | Na2CO3溶液中CO32-的水解:CO32-+H2O═HCO3-+OH- |
6.下列有关化学用语表示正确的是( )
| A. | 1,3-丁二烯的实验式:C4H6 | B. | 乙醇的分子式:C2H5OH | ||
| C. | 甲醛的结构式: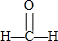 | D. | 聚丙烯的结构简式: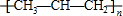 |
5.为了使CH3COONa溶液中Na+的浓度与CH3COO-的浓度比为1:1,可在CH3COONa溶液中加入( )
①适量的盐酸 ②适量的NaCl ③适量的醋酸 ④适量的CH3COONa.
①适量的盐酸 ②适量的NaCl ③适量的醋酸 ④适量的CH3COONa.
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
15.除去Na2CO3固体中混有少量NaHCO3固体的最佳方法( )
| A. | 加入盐酸 | B. | 通入CO2 | ||
| C. | 加热至固体质量不再减少为止 | D. | 加入NaOH溶液 |
2.离子检验的方法正确的是( )
| A. | 某溶液$\stackrel{+AgNO_{3}溶液}{→}$生成白色沉淀,说明原溶液中含有Cl- | |
| B. | 某溶$\stackrel{+HCl溶液}{→}$无现象$\stackrel{+BaCl_{2}溶液}{→}$生成白色沉淀,+说明原溶液中含有SO42- | |
| C. | 某溶$\stackrel{+NaOH溶液}{→}$生成红褐色沉淀,说明原溶液中含有Fe3+ | |
| D. | 某溶$\stackrel{+稀硫酸}{→}$生成无色气体,说明原溶液中含有CO32- |
19.下列实验方案不可行的是( )
| A. | 稀盐酸清洗做焰色反应的铂丝 | |
| B. | 金属钠保存在煤油中 | |
| C. | 用丁达尔现象区别溶液与胶体 | |
| D. | 除去粗盐溶液中的Ca2+、SO42-:先加Na2CO3溶液后加BaCl2溶液 |

 某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.
某课外小组分别用图所示装置对原电池和电解池原理进行实验探究.