2.下列实验装置能达到实验目的是( )


| A. | 实验Ⅰ:制备少量氧气 | |
| B. | 实验Ⅱ:比较酸性强弱:H2SO4>H2CO3>H2SiO3 | |
| C. | 实验Ⅲ:分离溴的苯溶液 | |
| D. | 实验Ⅳ:观察纯碱的焰色反应 |
1.将ag乙醇(分子式为C2H6O)充分燃烧,将燃烧生成的气体(150℃)通过盛有过量Na2O2的干燥管(反应气体无损失),充分反应后干燥管增重bg,则a和b的关系为( )
| A. | a>b | B. | a=b | C. | a<b | D. | 无法比较 |
20.下列物质不能通过化合反应制得的是( )
| A. | FeCl2 | B. | Mg3N2 | C. | Fe(OH)3 | D. | BaSO4 |
19.在三个密闭容器中分别充入Ne、N2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
| A. | p(Ne)>p(N2)>p(O2) | B. | p(O2)>p(Ne)>p(N2) | C. | p(N2)>p(O2)>p(Ne) | D. | p(N2)>p(Ne)>p(O2) |
18.下列工业生产中,用石灰石作为原料的是( )
①海水提镁②氯碱工业③制普通玻璃④工业制硫酸⑤制漂白粉⑥冶炼生铁⑦制硅酸盐水泥⑧工业制高纯硅.
①海水提镁②氯碱工业③制普通玻璃④工业制硫酸⑤制漂白粉⑥冶炼生铁⑦制硅酸盐水泥⑧工业制高纯硅.
| A. | ①③⑤⑥⑦ | B. | ①②⑤⑦⑧ | C. | ②③④⑤⑥ | D. | ①③⑥⑦⑧ |
17.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | Na2O2与CO2反应生成11.2LO2(标准状况),反应中转移的电子数为2NA | |
| C. | 在标准状况下,22.4LSO3所含的氧原子数目为3NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
16.下列物质按纯净物、混合物、电解质、非电解质顺序组合正确的一组为( )
| A. | 浓硫酸、空气、小苏打、乙醇 | B. | 生石灰、漂白粉、铁、二氧化硫 | ||
| C. | 明矾、盐酸、碳酸钙、氯气 | D. | 冰水混合物、氨水、纯碱、干冰 |
15.电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO${\;}_{3}^{-}$的原理如图所示,下列说法不正确的是( )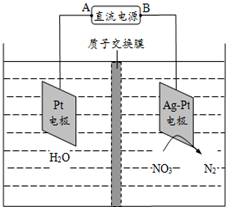
0 153560 153568 153574 153578 153584 153586 153590 153596 153598 153604 153610 153614 153616 153620 153626 153628 153634 153638 153640 153644 153646 153650 153652 153654 153655 153656 153658 153659 153660 153662 153664 153668 153670 153674 153676 153680 153686 153688 153694 153698 153700 153704 153710 153716 153718 153724 153728 153730 153736 153740 153746 153754 203614

| A. | 铅蓄电池的A极为正极,电极材料为PbO2 | |
| B. | 该电解池的阴极反应式为:2NO3-+12H++10e-═N2↑+6H2O | |
| C. | 该电解池的总反应方程式为:2H2O+4NO3-$\frac{\underline{\;电解\;}}{\;}$2N2↑+5O2↑+4OH- | |
| D. | 若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g |

 2NH3.
2NH3.